庄辉院士:扩大筛查 、提高诊断率和治疗率,加速消除乙型肝炎
—— 作者: 时间:2024-03-02
阅读数:
19
编者按
中国目前拥有超过7500万慢性乙型肝炎病毒(HBV)感染者,但令人担忧的是,仅有24%的患者被诊断出来,而仅有15%的患者接受了治疗[1]。这与世界卫生组织(WHO)提出的到2030年消除乙型肝炎危害的目标相去甚远。HBV感染筛查是减少乙型肝炎危害的关键措施之一。因此,扩大筛查范围,提高诊断率和治疗率,成为加速消除乙型肝炎的必由之路。北京大学基础医学院庄辉院士近期在学术交流中,以“扩大筛查、提高诊断率和治疗率,加速消除乙型肝炎”为题,进行了精彩的学术报告,系统介绍了筛查助力消除乙型肝炎的原因,以及我国消除乙型肝炎进展最新数据,并通过解析美国HBV筛查策略、成人筛查HBV的成本效益,深入剖析了我国HBV筛查的现状与挑战。《国际肝病》特将报告内容整理如下,以飨读者。
1
筛查是消除乙型肝炎的关键措施之一
HBV感染可导致慢性HBV感染、肝硬化和肝细胞癌(HCC);但20%的HCC患者是由慢性HBV感染(无肝硬化)直接发展而来[2]。HCC发病机制贯穿整个慢性HBV感染期;其直接机制为HBV DNA整合,间接机制包括宿主免疫力和炎症坏死/纤维化[2](图1)。
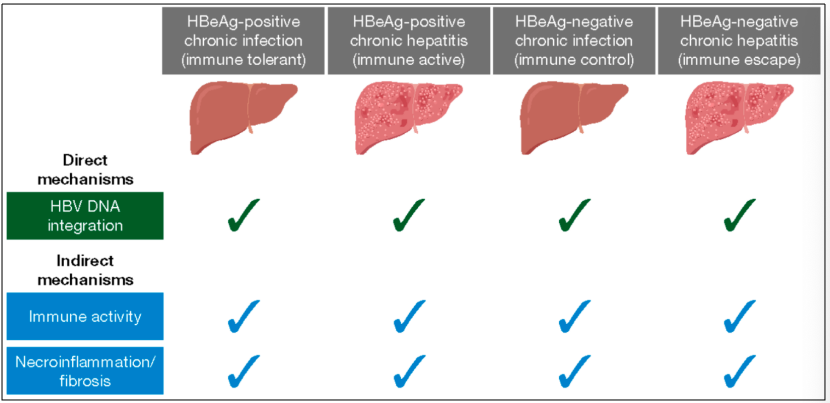
图1. HCC发病机制贯穿整个慢性HBV感染期(引自讲者幻灯)
筛查可提高诊断率和治疗率、降低死亡率[3-5]。通过筛查乙型肝炎表面抗原(HBsAg)、乙型肝炎核心抗体(抗-HBc)和乙型肝炎表面抗体(抗-HBs),对HBsAg阳性者作进一步诊断和治疗,并同时进行HCC监测,做到早发现、早根治;对上述3项标志物均阴性者接种乙型肝炎疫苗;对单项抗-HBc阳性者评价其再活动风险,确定在免疫抑制剂等治疗前是否需要预防性抗病毒治疗。因此,筛查可提高乙型肝炎的诊断率、治疗率,降低死亡率和发病率(图2)。

图2. HBV感染筛查流程(引自讲者幻灯)
根据2023年12月15日Polaris发布的我国消除乙型肝炎进展数据,我国慢性HBV感染人数达7974.2万,诊断率仅为24%,年治疗率仅为15%,乙型肝炎相关年死亡超过45万例,首针乙型肝炎及时接种率95%,3针乙型肝炎疫苗覆盖率99%,乙型肝炎免疫球蛋白(HBIG)覆盖率100%;然而高病毒载量孕妇治疗率仅为26%,需要进一步提高,以减少母婴传播[1]。
2020年北京CDC对本市16个区进行HBV感染随机抽样调查,共调查74 998人,25岁以上人群HBsAg流行率为 2.5%,对其中1929例HBsAg阳性者调查,既往确诊为乙型肝炎者654例,诊断率为33.9%;接受治疗者23例,占2.9%[6]。
有研究显示,中国HCC诊断时按巴塞罗那分期为中晚期的患者占67%,远远高于日、韩和中国台湾地区[7](图3)。由于初诊时大多数患者已处于中晚期,我国大陆地区HCC的 5年存活率仅为14.1%,远低于日、韩、中国台湾地区和澳大利亚,高于印度[8-12](图4)。这也再次强调诊断慢性HBV感染后,应同时进行HCC监测,做到早发现,早根治,提高HCC的 5年存活率。
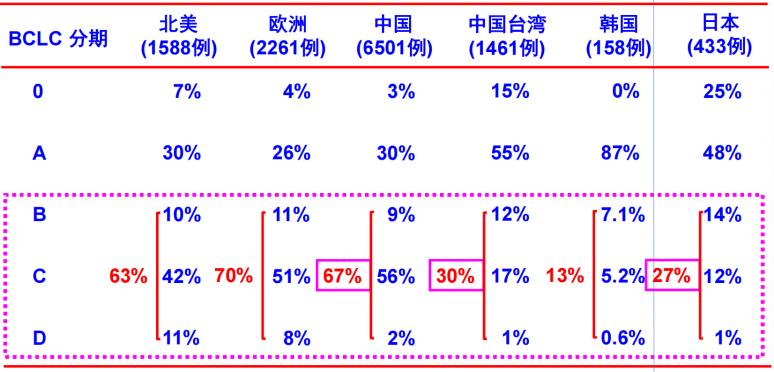
图3. 北美、欧洲、中国、中国台湾、韩国、日本HCC诊断时分期(引自讲者幻灯)
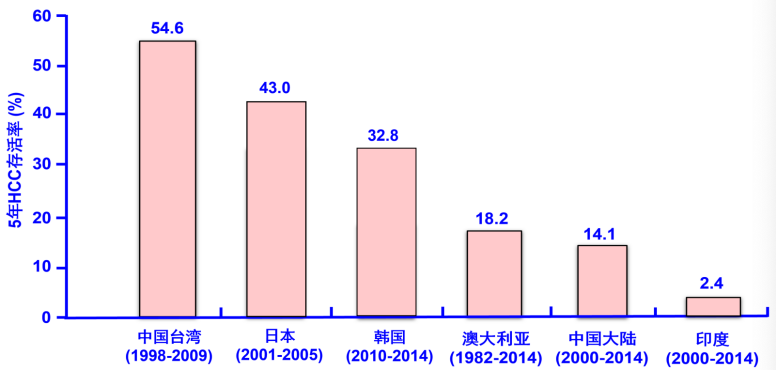
图4. 不同国家及地区HCC 的5年存活率(引自讲者幻灯)
2
筛查结果的解释及处理意见
2008年,美国尚未提出筛查的概念,在一篇关于慢性HBV感染者管理的报告[13]中,提出对HBsAg流行率≥2%地区人群、有暴露危险行为人群、接受免疫治疗或细胞毒素等治疗人群,以及患不明原因肝病患者进行HBV感染检测。2018年提出对以下2部分人进行筛查:所有孕妇进行HBsAg筛查;有高危因素的成年人,包括12类高危人群[14]。
2023年,美国疾病预防控制中心(CDC)首次出台专门针对HBV感染筛查和检测的推荐意见[4]。此次推荐意见保留了2018年提出的对孕妇和高危人群筛查的建议,另新增3条,即:① ≥18岁成人需要普遍筛查HBV感染;② 对任何有检测意愿的人进行筛查;③ 筛查3项HBV标志物(HBsAg、抗-HBs和抗-HBc)。HBV感染筛查结果及单项抗-HBc阳性结果解释及处理意见见表1和表2。
表1. HBV感染筛查结果解释和处理意见

(引自讲者幻灯)
表2. 单项抗-HBc阳性结果解释及处理意见

(引自讲者幻灯)
3
成人筛查乙型肝炎符合成本效益
从卫生经济学角度,美国一项针对现行筛查策略和普遍筛查策略进行的成本效益分析中,跟据未被诊断的慢性HBV感染流行率和HBV检测费用来分析筛查的成本效益。结果显示,估计未被诊断的慢性HBV感染流行率为0.24%,抗病毒治疗费用为每年894美元,对18~69岁人群普遍筛查符合成本效益(图5)[15]。所以,对流行率>0.24%的地区进行筛查是符合成本效益的。我国2020年乙型肝炎血清流行病学调查表明,我国HBV流行率为5.86%,远远高于0.24%,所以我国进行普遍筛查HBV感染也符合成本效益。此外,美国报告称,在成年人中,每筛查10万人,可使代偿期肝硬化发生率减少30%、失代偿期肝硬化减少43%、HCC减少23%、肝移植减少24%和HBV相关死亡减少27%(表3)[15]。
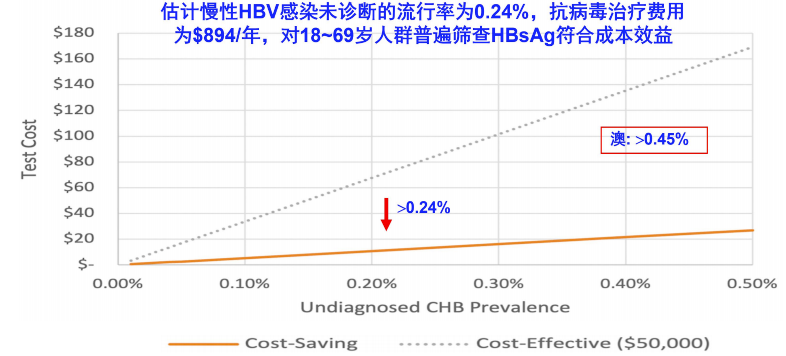
图5. 基于未被诊断的慢性HBV感染流行率和HBV检测费用分析筛查的成本效益(引自讲者幻灯)
注:增量成本效果比值(ICER)为50000美元/质量调整生命年被认为是符合成本效益
表3. 美国现行筛查和一次性普遍筛查HBsAg的临床预后和成本效益
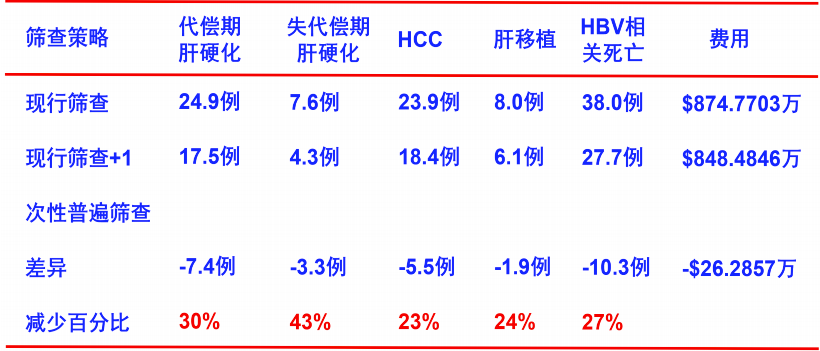
(引自讲者幻灯)
此外,筛查后的临床管理也至关重要,筛查后临床管理的比例越高,成本效益越好[16]。最新数据显示,与现行HBV筛查策略比较,普遍筛查联合筛查后50%临床管理,至2030年,新发HCC将减少7.3%,慢性乙型肝炎死亡将减少8.5%,累计HBV相关死亡将减少5%(表4)[17]。
表4. 至2030年普遍筛查+50%临床管理的临床预后和成本效益
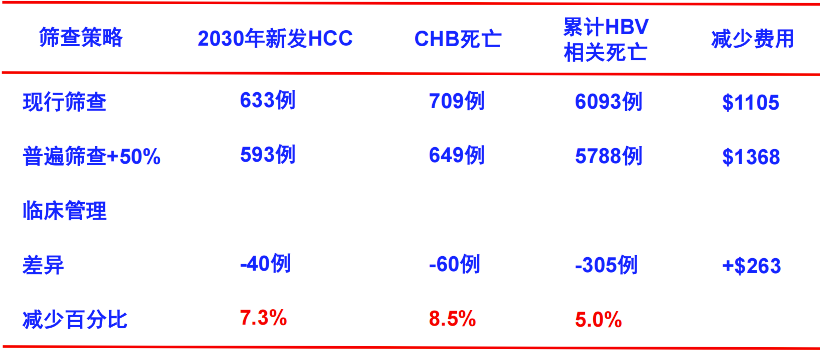
(引自讲者幻灯)
4
我国HBV感染筛查的现状与挑战
早在2017年,国务院11个部委联合发布的《中国病毒性肝炎防治规划(2017~2020年)》中,就对HBV感染检测提出5点要求,包括完善检测策略、医院检测、纳入健康体检范畴、对检查发现的阳性者要提供必要的诊断和抗病毒治疗等。然而,文件大部分要求至今仍未能完全落实,最关键的是:筛查后缺乏必要的诊断和治疗。
据统计[18],2016~2017年间,我国参与HBV感染筛查的人群已达7.6亿人次,其中产前检查孕妇人群1847万人,接受外科手术患者5080万例,住院患者2.4亿例次,血透析患者59.6万例,冠心病介入治疗患者56.7万例,接受健康体检人群4.19亿人次,献血员筛查为2459万人。但筛查之后的诊断和治疗疗没有跟上。
我国最新版《慢性乙型肝炎防治指南(2022年版)》(下称“指南”)对HBV感染筛查也给出了明确建议[19]:对一般人群均应该进行HBsAg筛查,特别是HIV感染者、男男性行为者、静脉药瘾者、HBV感染者的性伴侣和家庭接触者、接受免疫抑制剂或抗肿瘤药物、抗丙型肝炎病毒(HCV)药物治疗者等,以及孕妇和育龄期、备孕期女性等。但① 未提及对于愿意检测者进行筛查;② 仅提出筛查HBsAg,③ 未提筛查3项HBV感染指标(HBsAg、抗-HBs和抗-HBc),④没有明确提出对筛查后人群进行及时的诊断和治疗。
小结
HBV感染筛查的普及有助于进一步提高乙型肝炎的诊断率和治疗率,是消除乙型肝炎的关键措施之一。同时,扩大HBV感染筛查符合成本效益,因此,我国需要尽快制定普遍筛查HBV感染的策略和具体建议。
参考文献:
1. Polaris Observatory Collaborators. Global prevalence, cascade of care, and prophylaxis coverage of hepatitis B in 2022: a modelling study. Lancet Gastroenterol Hepatol, 2023, 8(10):879-907.
2. Lim YS, Kim WR, Dieterich D, et al. Evidence for benefits of early treatment initiation for chronic hepatitis B. Viruses, 2023, 15(4):997.
3. So S, Terrault N, Conners EE. Universal adult hepatitis B screening and vaccination as the path to elimination. JAMA, 2023, 329(19):1639-1640.
4. Conners EE, Panagiotakopoulos L, Hofmeister MG, et al.Screening and testing for hepatitis B virus infection: CDC recommendations - United States, 2023. MMWR Recomm Rep, 2023, 72(1):1-25.
5. Su TH, Kao JH. Improving clinical outcomes of chronic hepatitis B virus infection. Expert Rev Gastroenterol Hepatol, 2015, 9(2):141-154.
6. 北京CDC吴疆研究员提供 (2023.10).
7. Park JW, Chen M, Colombo M, et al. Global patterns of hepatocellular carcinoma management from diagnosis to death: the BRIDGE Study. Liver Int, 2015, 35(9):2155-2166.
8. Allemani C, Matsuda T, Di Carlo V, et al. Global surveillance of trends in cancer survival 2000-14 (CONCORD-3): analysis of individual records for 37?513?025 patients diagnosed with one of 18 cancers from 322 population-based registries in 71 countries. Lancet, 2018, 391(10125):1023-1075.
9. Chiu CC, Wang JJ, Chen YS, et al. Trends and predictors of outcomes after surgery for hepatocellular carcinoma: A nationwide population-based study in Taiwan. Eur J Surg Oncol, 2015, 41(9):1170-1178.
10. Wallace MC, Preen DB, Short MW, et al. Hepatocellular carcinoma in Australia 1982-2014: Increasing incidence and improving survival. Liver Int, 2019, 39(3):522-530.
11. Kudo M. Surveillance, diagnosis, treatment, and outcome of liver cancer in Japan. Liver Cancer, 2015, 4(1):39-50.
12. Yoo SH, Kim SS, Kim SG, et al. Current status of ultrasonography in national cancer surveillance program for hepatocellular carcinoma in South Korea: A large-scale multicenter study. J Liver Cancer, 2023, 23(1):189-201.
13. Weinbaum CM, Williams I, Mast EE, et al. Recommendations for identification and public health management of persons with chronic hepatitis B virus infection. MMWR Recomm Rep, 2008, 57(RR-8):1-20.
14. Schillie S, Vellozzi C, Reingold A, et al. Prevention of hepatitis B virus infection in the United States: Recommendations of the Advisory Committee on Immunization Practices. MMWR Recomm Rep, 2018, 67(1):1-31.
15. Toy M, Hutton D, Harris AM, et al. . Cost-effectiveness of 1-time universal sscreening for chronic hepatitis B infection in adults in the United States. Clin Infect Dis, 2022, 74(2):210-217.
16. Tran L, Cowie BC. Universal testing for hepatitis B must be accompanied by better linkage with care. Med J Aust, 2023, 218(4):165-166.
17. Xiao Y, Hellard ME, Thompson AJ, et al. The cost-effectiveness of universal hepatitis B screening for reaching WHO diagnosis targets in Australia by 2030. Med J Aust, 2023, 218(4):168-173.
18. National viral hepatitis prevention and control plan(2017–2020). Beijing: Department of Disease Prevention and Control, National Health Commission of the People's Republic of China; 2017. Chinese. Available from: http://www.nhfpc.gov.cn/ewebeditor/uploadfile/2017/11/20171113134002475.pdf
19. 中华医学会肝病学分会,中华医学会感染病学分会.
慢性乙型肝炎防治指南(2022年版).中华肝脏病杂志,2022, 29(12):1309-1331.
(来源:《国际肝病》编辑部)

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
标签:
访谈
专家访谈
乙肝
发表评论
全部评论
