年度盘点丨窦晓光教授:病毒性肝炎临床相关重要进展
—— 作者: 时间:2024-02-15
阅读数:
18
编者按
随着新年的到来,世界卫生组织(WHO)“2030消除病毒性肝炎公共危害”目标进入到6年倒计时。2024年2月,中国医科大学附属盛京医院窦晓光教授应邀在“肝脏疾病2023年度前沿进展研讨会”上,回顾病毒性肝炎领域在过去一年中的重要临床研究,主要包括疫苗预防、感染筛查、早期诊断、早期治疗和抗病毒治疗新药的临床研发,为新一年如何助力达成目标提供指引。
01
全人群乙型肝炎病毒(HBV)感染筛查,以实现早期诊断和及时治疗
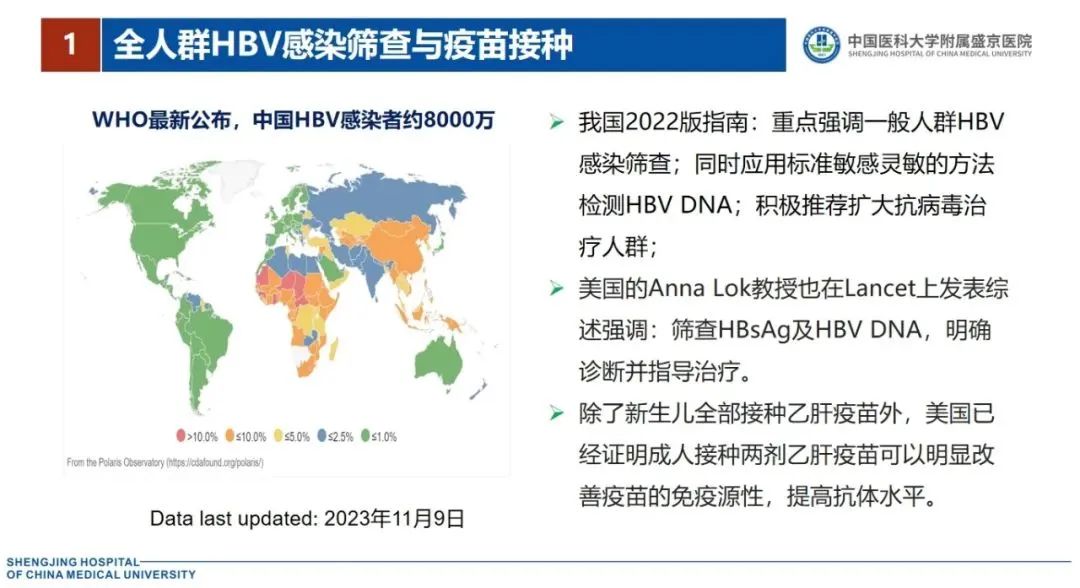
HBV感染仍然是严重危害人类健康的公共健康问题。2019年,全球HBV相关肝硬化死亡病例高达331 000人,肝细胞癌(HCC)患者更是高达192 000例。其主要原因是感染者没有得到及时诊断和治疗[1]。据Polaris 2023年12月15日报告数据:全球乙型肝炎诊断率仅14%,治疗率仅8%,诊断率和治疗率均非常低[2]。
2023年,我国《慢性乙型肝炎防治指南(2022年版)》于《中华肝脏病杂志》和Journal of Clinical and Translational Hepatology发布,得到了国内外特别是WHO的一致好评。指南重点强调一般人群HBV感染筛查、应用灵敏方法检测HBV DNA,并积极推荐扩大抗病毒治疗人群,以使更多的慢性HBV感染者符合抗病毒治疗指征。相信只有经过这些措施的实施,才能实现消除CHB的目标[3]。
同样,美国密歇根大学Anna Lok教授也在顶刊《柳叶刀》(The Lancet)杂志上发表综述,强调应筛查HBsAg和HBV DNA,以明确诊断并指导治疗。除新生儿应全部接种乙型肝炎疫苗(乙肝疫苗)外,成人接种乙肝疫苗可显著降低成人乙型肝炎发病率,符合成本效益。她还强调,尽管目前临床应用的聚乙二醇干扰素α(Peg-IFN-α)和核苷(酸)类似物(NAs)抗病毒治疗可延缓或阻止疾病进展为肝硬化和HCC,但不能在短期内彻底清除病毒和HBsAg。因此,肝炎活动或疾病进展患者应积极抗病毒治疗[4-5]。
(图引自讲者幻灯)
02
慢性乙型肝炎治疗新药及治疗策略
2023年,欧洲肝脏研究学会(EASL)年会和美国肝病研究学会(AASLD)年会报告了众多慢性乙型肝炎(CHB)新药相关II期或III期临床试验进展,其结果提示:尽管在抑制病毒或降低HBsAg水平上显示不错的疗效,但均很难在短期内使CHB患者达到临床治愈[6]。
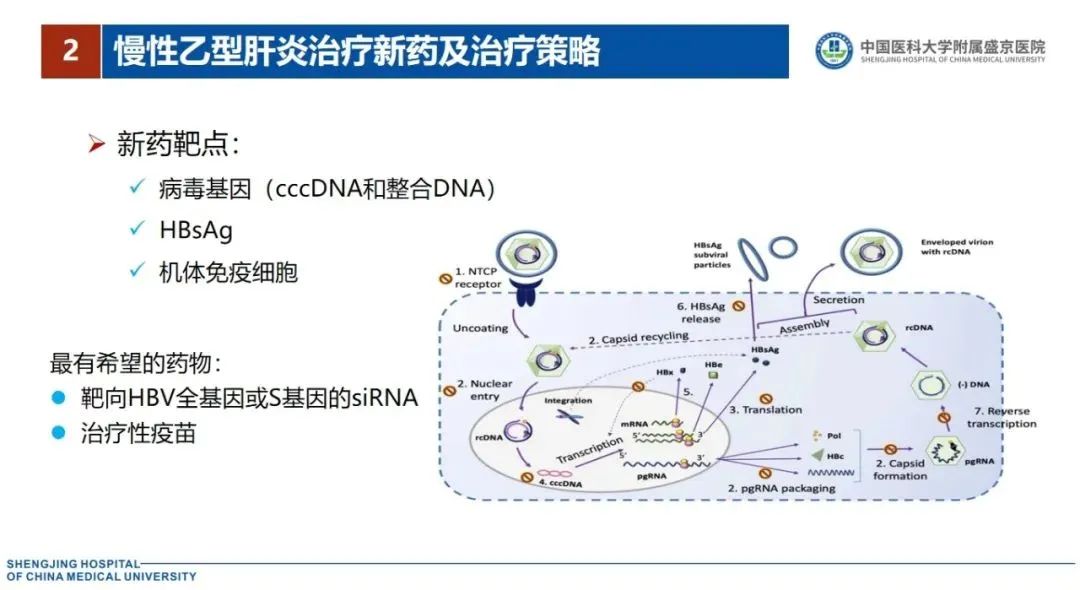
目前乙型肝炎新药靶点包括病毒基因(cccDNA和整合DNA)、HBsAg和机体免疫细胞。其中,治疗性疫苗包括蛋白疫苗、核酸疫苗和T细胞表位多肽疫苗等。研究者通过生物技术增强其免疫源性,同时提高机体细胞免疫功能。研究显示其可以有效地刺激HBV携带者或CHB患者免疫系统,打破免疫耐受(激活免疫应答),达到抑制和清除病毒的目的。
小干扰 RNA(siRNA)类药物研究较多,如Xalnesiran(RG6346)。其是靶向HBV基因组S区GalNAc结合的双联siRNA,开展了全球首个CHB和健康对照临床研究。结果显示,治疗后HBsAg下降明显且持久,且不受HBeAg状态影响。因其安全性和有效性高,有可能成为CHB功能性治愈的骨干药物[7-8]。VIR-2218(siRNA)靶向HBV全部主要转录基因,研究结果显示CHB患者接受治疗后 HBsAg下降明显 [9]。
然而,单一靶点药物均不能在短期内实现临床治愈,更难以获得彻底治愈(彻底清除cccDNA和整合DNA)。因此,治愈CHB合理的策略是不同靶点的药物联合治疗,例如 NAs或Peg-IFN-α联合siRNA及Toll样受体激动剂等免疫制剂[10]。
总之,目前控制HBV感染仍需依靠全面接种乙肝疫苗、扩大筛查、早期诊断与治疗的策略。期待乙型肝炎治愈新药尽早应用于临床,助力实现WHO 2030消除HBV感染公共卫生危害的目标[11]。
(图引自讲者幻灯)
03
消除丙型肝炎策略及其疫苗的研发与应用
直接抗病毒药物(DDAs)上市后,95%以上的接受治疗的患者可以在短期内获得治愈,丙型肝炎病毒(HCV)感染相关死亡人数明显下降,给消除丙型肝炎危害提供了很多机遇。但全球仍有80%的HCV感染者没有被诊断,仅靠抗病毒治疗不能彻底根除全球范围内的HCV感染,消除HCV感染仍面临很多挑战。筛查、转诊及治疗,特别关注高风险人群反复感染,至关重要[12]。欧美国家均已提出了消除丙型肝炎计划,以彻底消除HCV感染[13-14]。
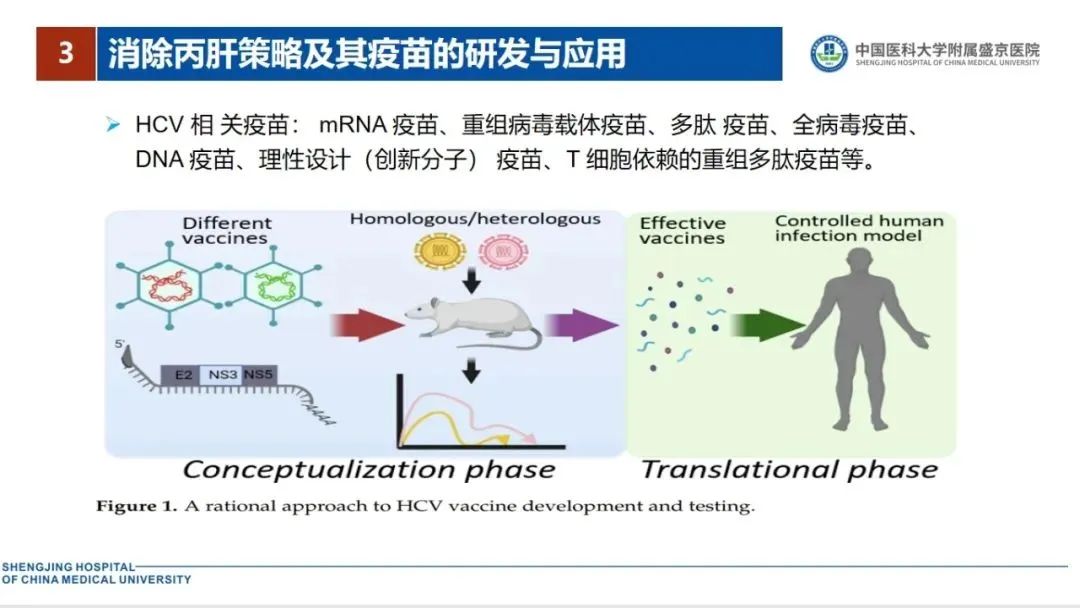
此外,想彻底消除HCV感染,也亟需丙型肝炎疫苗来减少疾病负担和预防HCV感染。目前,HCV相关疫苗包括mRNA疫苗、重组病毒载体疫苗、多肽疫苗、全病毒疫苗、DNA 疫苗、理性设计(创新分子)疫苗、T 细胞依赖的重组多肽疫苗等。最近研究提示可诱导中和抗体的HCV非结构蛋白的病毒载体T-细胞疫苗,可能会是未来的候选疫苗。诱导中和抗体的疫苗必须包括E1和E2蛋白的抗体[15-16]。在研究疫苗的同时,应强调丙型肝炎疫苗临床研究设计规范及其相应考核终点,以及确定接种人群、监测项目及安全性评价[17-18]。
尽管目前已经有很多丙型肝炎疫苗进行了临床研究,但尚无有效的保护性疫苗,主要原因是基因多态性、没有相关免疫组分的小动物模型、缺乏丙型肝炎疫苗接种后检测、没有体外病毒培养的组织细胞,以及没有完全阐明针对HCV感染的免疫应答机制等[19]。
(图引自讲者幻灯)
04
甲型和戊型肝炎相关研究
甲型肝炎和戊型肝炎多为急性自限性肝炎,然而在脆弱人群,包括孕妇、免疫功能低下人群或有基础肝病人群可发生重症、慢性肝炎。甲型肝炎病毒(HAV)感染偶尔可以引起重症肝炎、持续性胆汁淤积或复发性肝炎,并可诱发自身免疫性肝炎。戊型肝炎病毒(HEV)感染少见的临床表现包括肝外疾病、急性肝衰竭和持续病毒血症的慢性HEV感染。
尽管目前尚无特效抗HAV的药物,一些小分子药物,如JAK2抑制剂AZD 1480、氯化锌和血红素加氧酶等,体外证实其可以抑制病毒复制[20]。对于HEV感染可以应用利巴韦林和Peg-IFN-α[21]。特殊人群慢性HEV感染在增加,是否可以用抗HCV的小分子药物治疗HEV感染,特别是慢性戊型肝炎是目前探索的问题。有研究发现,索磷布韦联合利巴韦林可以抑制慢性戊型肝炎患者病毒复制,但疗效不够理想[22]。
此外,我们还要关注HAV/HEV双重和同时感染的问题。由于HAV和HEV均为单股RNA病毒,且有相同的传播途径,应关注两者同时感染的预后问题。尽管患者的临床表现与单独感染相似,但同时感染的患者可以发生重症肝炎,病死率明显高于单独感染患者[23]。

(图引自讲者幻灯)
05
肝炎病毒多方位快速检测新技术
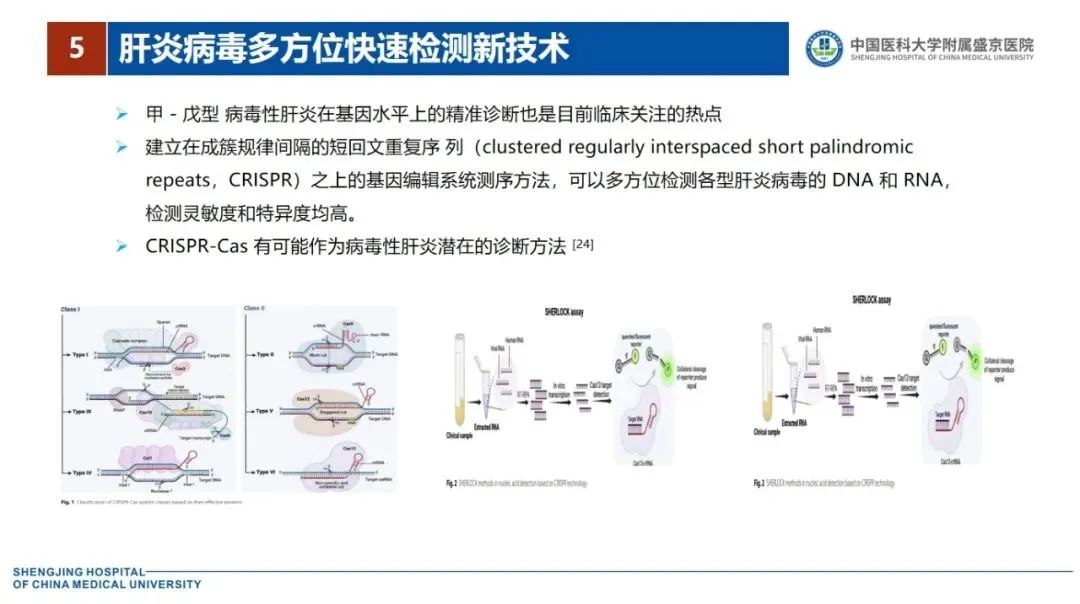
甲-戊型病毒性肝炎在基因水平上的精准诊断是目前临床关注的热点,建立在成簇规律间隔的短回文重复序列(CRISPR)之上的基因编辑系统测序方法,可以多方位检测各型肝炎病毒的DNA和RNA,检测灵敏度和特异度均高。CRISPR-Cas有可能作为病毒性肝炎潜在的诊断方法[24]。
(图引自讲者幻灯)
*以上内容综合整理自《中华肝脏病杂志》
参考文献:
[1] Hsu YC, Huang DQ, Nguyen MH. Global burden of hepatitis B virus: current status, missed opportunities and a call for action[J].Nat Rev Gastroenterol Hepatol, 2023, 20(8):524-537. DOI: 10.1038/s41575-023-00760-9.
[2] CDA Foundation. HBV infection[EB/OL]. (2023-12-15). https://cdafound.org/dashboard/polaris/dashboard.html.
[3] You H, Wang F, Li T, et al. Guidelines for the prevention and treatment of chronic hepatitis B (version 2022)[J]. J Clin Transl Hepatol, 2023, 11(6):1425-1442. DOI: 10.14218/JCTH.2023.00320.
[4] Jeng WJ, Papatheodoridis GV, Lok ASF. Hepatitis B[J]. Lancet, 2023, 401(10381):1039-1052. DOI: 10.1016/S0140-6736(22)01468-4.
[5] Lim YS, Kim WR, Dieterich D, et al. Evidence for benefits of early treatment initiation for chronic hepatitis B[J]. Viruses, 2023, 15(4):997. DOI: 10.3390/v15040997.
[6] Ogunnaike M, Das S, Raut SS, et al. Chronic hepatitis B infection: new approaches towards cure[J]. Biomolecules, 2023, 13(8):1208. DOI: 10.3390/biom13081208.
[7] Lim SG, Baumert TF, Boni C, et al. The scientific basis of combination therapy for chronic hepatitis B functional cure[J]. Nat Rev Gastroenterol Hepatol, 2023, 20(4):238-253. DOI: 10.1038/s41575-022-00724-5.
[8] Gane EJ, Kim W, Lim TH, et al. First-in-human randomized study of RNAi therapeutic RG6346 for chronic hepatitis B virus infection[J]. J Hepatol, 2023, 79(5):1139-1149. DOI: 10.1016/j.jhep.2023.07.026.
[9] Gane E, Lim YS, Kim JB, et al. Evaluation of RNAi therapeutics VIR-2218 and ALN-HBV for chronic hepatitis B: results from randomized clinical trials[J]. J Hepatol, 2023, 79(4):924-932. DOI: 10.1016/j.jhep.2023.05.023.
[10] Zoulim F, Testoni B. Eliminating cccDNA to cure hepatitis B virus infection[J]. J Hepatol, 2023, 78(4):677-680. DOI: 10.1016/j.jhep.2023.01.017.
[11] Yardeni D, Chang KM, Ghany MG. Current best practice in hepatitis b management and understanding long-term prospects for cure[J]. Gastroenterology, 2023, 164(1):42-60.e6. DOI: 10.1053/j.gastro.2022.10.008.
[12] Taha G, Ezra L, Abu-Freha N. Hepatitis C elimination: opportunities and challenges in 2023[J]. Viruses, 2023, 15(7):1413. DOI: 10.3390/v15071413.
[13] Berk J, Litwin A, Murphy M. US hepatitis C elimination plan[J]. JAMA, 2023, 330(9):877-878. DOI: 10.1001/jama.2023.11757.
[14] American Association for the Study of Liver Diseases. The national hepatitis C elimination program-AASLD's coalition and call to action[J]. Hepatology, 2023, 78(2):371-374. DOI: 10.1097/HEP.0000000000000444.
[15] Gomez-Escobar E, Roingeard P, Beaumont E. Current hepatitis C vaccine candidates based on the induction of neutralizing antibodies[J]. Viruses, 2023, 15(5):1151. DOI: 10.3390/v15051151.
[16] Shoukry NH, Cox AL, Walker CM. Immunological monitoring in hepatitis C virus controlled human infection model[J]. Clin Infect Dis, 2023, 77(Suppl 3):S270-S275. DOI: 10.1093/cid/ciad359.
[17] Feld JJ, Bruneau J, Dore GJ, et al. Controlled human infection model for hepatitis C virus vaccine development: trial design considerations[J]. Clin Infect Dis, 2023, 77(Suppl 3):S262-S269. DOI: 10.1093/cid/ciad362.
[18] Offersgaard A, Bukh J, Gottwein JM. Toward a vaccine against hepatitis C virus[J]. Science, 2023, 380(6640):37-38. DOI: 10.1126/science.adf2226.
[19] Adugna A. Therapeutic strategies and promising vaccine for hepatitis C virus infection[J]. Immun Inflamm Dis, 2023, 11(8):e977. DOI: 10.1002/iid3.977.
[20] Gabrielli F, Alberti F, Russo C, et al. Treatment options for hepatitis A and E: a non-systematic review[J]. Viruses, 2023, 15(5):1080. DOI: 10.3390/v15051080.
[21] Gabrielli F, Alberti F, Russo C, et al. Treatment options for hepatitis a and e: a non-systematic review[J]. Viruses, 2023, 15(5):1080. DOI:10.3390/v15051080.
[22] Gouttenoire J, Neyts J. Toward antivirals against hepatitis E: in the steps of hepatitis C[J]. Hepatology, 2023, 78(6):1695-1697. DOI:10.1097/HEP.0000000000000509.
[23] Sayed IM. Dual infection of hepatitis A virus and hepatitis E virus-What is known?[J]. Viruses, 2023, 15(2):298. DOI: 10.3390/v15020298.
[24] Bahrulolum H, Tarrahimofrad H, Rouzbahani FN, et al. Potential of CRISPR/Cas system as emerging tools in the detection of viral hepatitis infection[J]. Virol J, 2023, 20(1):91. DOI: 10.1186/s12985-023-02048-5.

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
标签:
访谈
专家访谈
其他肝病
发表评论
全部评论
