当前位置:AASLD-美国肝病研究学会年会 » 正文
AASLD中国之声丨 北京大学肝病研究所10项成果闪耀2023美肝会
—— 作者: 时间:2023-11-11 11:46:27 阅读数:
18

编者按
2023年11月10日~14日,肝病学领域国际年度压轴大戏——美国肝病研究学会年会(AASLD2023)于美国波士顿隆重举行。据不完全统计,我国专家学者有200余篇摘要入选本届大会口头报告或壁报交流,成果丰硕,在此表示热烈祝贺!
北京大学人民医院、北京大学肝病研究所团队围绕肝性脑病、脂肪肝、丙型肝炎、乙型肝炎和肝癌领域的科学研究,喜获1篇oral和9篇poster。部分研究摘要分享如下,《国际肝病》带您一睹团队风采。

01
中性粒细胞/淋巴细胞比值预测肝性脑病患者的短期和长期再入院风险
3092-A | Neutrophil-to lymphocyte ratio predicts short- and long- term readmission of patients with hepatic encephalopathy
作者:黄睿,张琳
通讯作者:黄睿
研究背景
肝性脑病(hepatic encephalopathy, HE)是肝病晚期的重要并发症,预示着不良预后。肝硬化患者的30天和90天的再入院率为20%~30%,最常见的原因就是肝性脑病。已有报道指出多种因素是HE患者再入院的预测因素。然而,除肝功能指标外,鲜有发现新的血清指标可以预测HE患者的再入院。为了探索肝性脑病患者短期和长期再入院的简单有效的预测因子,我们进行了这项回顾性研究。
研究方法
我们进行了一项单中心的回顾性研究,纳入因HE入院的患者。主要终点是30天、90天和180天内首次肝脏相关再入院。应用logistic回归分析和多元线性回归分析,统计与再入院和首次住院时长相关的预测因子。
研究结果
我们纳入了424名因HE入院的患者,在30天、90天和180天内,分别有24例(5.7%)、63例(14.8%)和92例(21.7%)患者再次入院。在这些患者中,283例(66.7%)为男性,平均年龄为59.9 ± 11.5岁。120例(28.3%)患者患有酒精性肝硬化。在基线时,有40例(9.4%)、246例(58.0%)、67例(15.8%)和20例(4.7%)患者分别伴有肝细胞癌(hepatocellular carcinoma, HCC)、腹水、静脉曲张出血和自发性细菌性腹膜炎(spontaneous bacterial peritonitis, SBP)。
180天内再次入院的患者年龄较大(62.0 ± 9.6 vs. 59.3 ± 12.0, P=0.025),无医疗保险比例较高[25(27.2%) vs. 52(15.7%), P=0.010]酒精性肝病(alcoholic liver disease, ALD)比例较高[34(37.0%) vs. 86(25.9%), P=0.027],慢性肾脏病(chronic kidney disease, CKD)比例较高[21(22.8%) vs. 39(11.7%), P=0.007],HCC比例较高(15(16.3%) vs. 25(7.5%), P=0.012),腹水比例较高(65(70.7%) vs. 181(54.5%), P=0.004)。患者入院原因除了HE外,还包括容量相关(247例,58.3%)和其他并发症(177例,41.7%)。所有患者首次住院的平均住院时间为17.9 ± 12.1天。
HE是再入院最常见的原因,在30天、90天和180天内,分别有15例(62.5%)、30例(47.6%)和48例(52.1%)患者因HE再次入院。此外,与30天、90天或180天内未再入院的患者相比,再入院患者在首次出院时的中性粒细胞/淋巴细胞比值(neutrophil-to-lymphocyte ratio, NLR)较高(8.17 ± 12.1 vs. 3.95 ± 4.96; 7.17 ± 9.72 vs. 3.67 ± 4.44; 6.80 ± 8.62 vs. 3.47 ± 4.28, P<0.001)。30天内再次入院的患者在首次住院期间的住院时间最长,显著高于30天内未再入院的患者(24.8 ± 19.2 vs. 17.7 ± 11.90, P<0.001)。
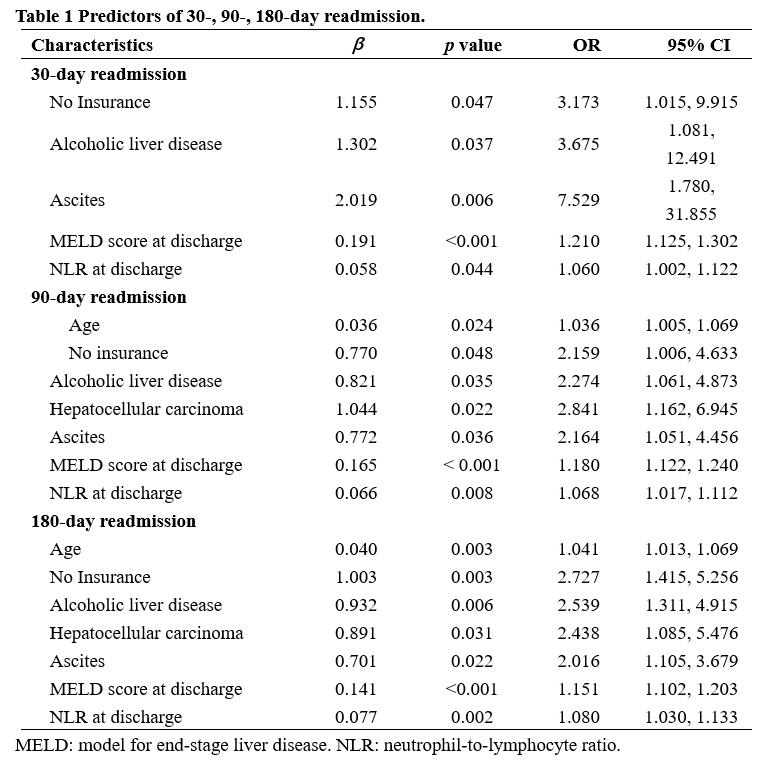
Logistic 回归分析显示,显著的再入院预测因素包括无医疗保险、ALD、腹水、MELD评分和首次出院时的NLR。年龄和HCC也是90天和180天再入院的显著预测因素(表1)。然而,再入院的预测因素中存在性别差异。在男性中,除了HCC、腹水、MELD 评分和出院时的 NLR 外,ALD 对短期和长期再入院都是显著的预测因素。有趣的是,在女性中,ALD不是再入院的显著预测因子,而高血压与180天再入院显著相关。首次住院时长的显著预测因素包括首次入院时静脉曲张出血(P=0.006)、CKD(P=0.003)和出院时的 MELD 评分(P=0.024)。
研究结论
出院时的 NLR是HE患者短期和长期再入院的显著预测因子。CKD是影响HE患者首次住院时长的显著因素。
表1. 30天、90天和180天再入院的再预测因素
通讯作者简介

黄睿
北京大学医学博士,北京大学人民医院、北京大学肝病研究所、肝病科副主任医师。参与20余项国家/省部级科研项目和全球/全国多中心药物临床试验。主持北京大学人民医院研究与发展基金1项。以第一/通讯作者发表论文10余篇,其中SCI论文9篇。获2022年北京市科学技术奖二等奖(第四完成人)。获2019年欧洲肝病学会青年研究者奖。GUT中文版青年编委,Quality of Life Research、Frontiers in Medicine审稿人。
02
持续病毒学应答改善慢性丙型肝炎患者的长期健康相关生活质量——一项全国多中心前瞻性研究
1856-A | Sustained Virologic Response Improved the Long term Health-Related Quality of Life In Patients With Chronic Hepatic C: A Prospective National Study In China
作者:黄睿,饶慧瑛
通讯作者:饶慧瑛
研究背景
慢性丙型肝炎病毒(chronic hepatitis C virus, HCV)感染会严重影响患者的健康相关生活质量(health-related quality of life, HRQoL)。虽然已知持续病毒学应答(sustained virologic response, SVR)有助于改善HRQoL,但目前在真实世界环境中缺乏长期随访的前瞻性研究。我们进行了一项全国多中心前瞻性研究,以调查HCV感染者的HRQoL变化趋势,并评估抗病毒治疗对其的长期影响。
研究方法
我们在全国28家医院进行了一项前瞻性观察性研究(CCgnos研究的一部分),对象为被诊断患有慢性HCV感染的成年患者。收集了患者的社会人口学、临床特征以及EQ-5D问卷调查数据。为了评估这些变量与HRQoL随时间变化之间的关系,我们应用了广义估计方程(generalized estimating equation, GEE)模型。
研究结果
研究纳入了456名患者,中位年龄为46.5(36.5~57.0)岁,262名(57.5%)为男性,44名(9.6%)患有肝硬化。主要的HCV基因型为基因型1(46.1%)和基因型2(25.4%)。基线时的对数HCV RNA为6.10(5.34, 6.55)IU/mL。在335名接受抗病毒治疗(干扰素和利巴韦林治疗)的患者中,73.5%在随访结束前获得了SVR24。基线EQ-5D指数和EQ-VAS评分分别为0.916 ± 0.208和80.6 ± 13.0。
在基线时,获得SVR和没有获得SVR的患者的EQ-5D指数没有显著差异(0.959 ± 0.077 & 0.913 ± 0.215,P 0.241),从第一年开始,SVR组的EQ-5D指数和EQ-5D VAS分数均显著高于无SVR组,然而到了第五年,这种组间差异不再显著。EQ-5D指数和EQ-VAS每年都有所增加,随着时间的推移,报告在EQ-5D五个维度的任何一个维度中存在中重度不适的患者比例逐渐减少。图1显示了在随访期间报告在EQ-5D各维度中存在中重度问题的患者数量。
按照SVR状态进行分层,随着时间的推移,获得SVR和没有获得SVR的患者之间的差异变得显著,特别是在MO和UA两个维度[第五年:MO:8(4.8%)和8(18.6%),P=0.032;UA:4(2.4%)和7(16.3%),P=0.021]。此外,没有获得SVR的患者报告疼痛或不适的比例显著高于获得SVR的患者[第一年:21(12.2%)和39(23.9%),P=0.005;第二年:20 (9.9%)和39(20.2%),P=0.000;第三年:29(15.3%) 和28(25.0%),P=0.047;第四年:19(10.9%)和18(22.8%),P=0.027]。
使用GEE模型分析HCV感染者纵向EQ-5D指数和EQ-VAS的预测因素。单变量分析显示性别、年龄、居住地、婚姻状况、教育程度、收入、肝硬化、贝克抑郁评分和随访持续时间与EQ-5D指数显著相关。此外,获得SVR24与EQ-5D指数呈正相关[β=0.049,95%CI:0.033~0.065,P=0.000]。性别、年龄、居住地、婚姻状况、教育程度、收入、肝硬化、基因型和随访持续时间是EQ-VAS的显著预测因素。同时,SVR24是EQ-VAS的纵向强预测因素[β=5.933,95%CI(4.827~7.040),P=0.000]。
多变量分析显示,年龄、收入和SVR24[β=0.040,95% CI:0.023~0.057,P=0.000]是EQ-5D指数的显著预测因素,而性别、年龄、基因型和SVR24[β=5.333,95%CI:4.204~6.462,P=0.000]与EQ-VAS随时间变化相关。
研究结论
我们的研究表明,通过抗病毒治疗实现病毒清除可以改善HCV患者的长期HRQoL。特定的社会人口统计学因素,以及肝硬化和基因型的存在,也显著影响了患者生活质量的长期变化。
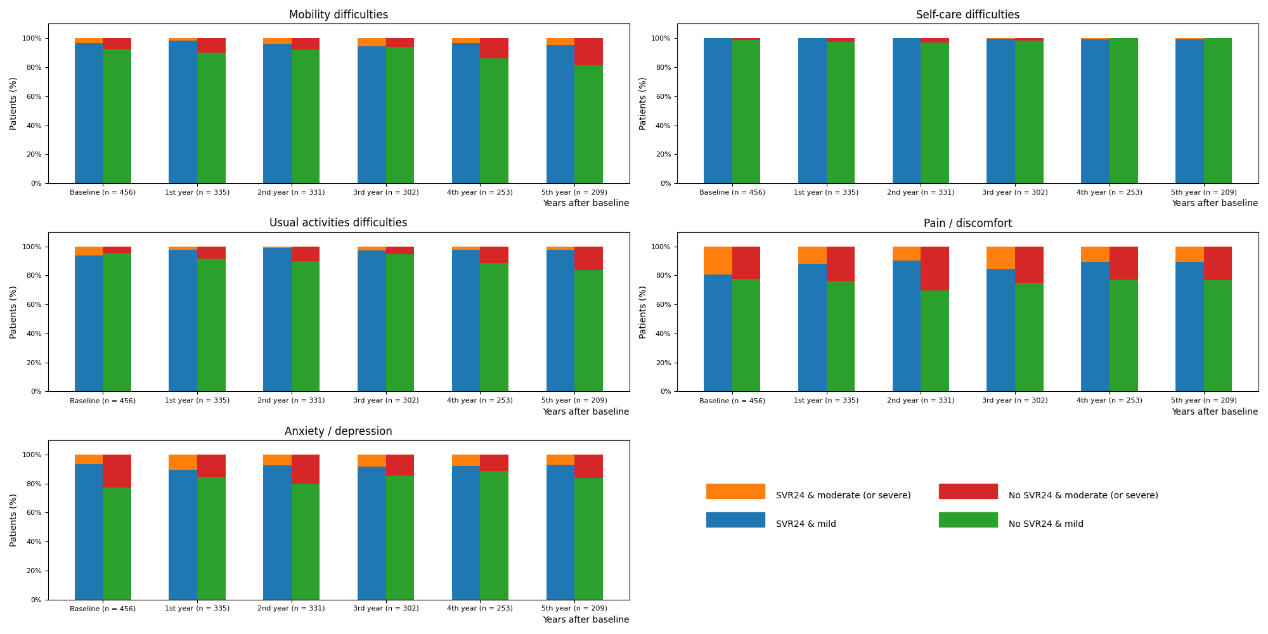
图1. 随访期间报告在EQ-5D各维度中存在中重度问题的患者数量变化
03
揭示可能预测非酒精性脂肪性肝病合并肝纤维化进展为肝细胞癌风险的新型关键基因
2053-A | Identification of Novel Hub Genes that may Predict the Risk of Liver Fibrosis Progressing to Hepatocellular Carcinoma In Non-Alcoholic Fatty Liver Disease
第一作者:刘百怡
通讯作者:饶慧瑛
研究背景
非酒精性脂肪性肝病(NAFLD)是世界范围内最常见的慢性肝病,包括非酒精性脂肪变性、非酒精性脂肪性肝炎、肝纤维化和肝硬化。如果不干预NAFLD纤维化,肝脏可进一步发展为肝细胞癌(HCC)。近年来,随着NAFLD患者数量的不断增加,NAFLD越来越被认为是HCC的一个促成因素,而肝纤维化是HCC的一个关键阶段。目前,NAFLD的诊断方法有很多,包括无创评估和有创评估,例如B超、MRE、FIB-4、FAST评分以及肝脏组织活检等。
尽管这些临床检查对NAFLD及其各个阶段的诊断提供了有效的帮助,但并不能预测NAFLD合并肝纤维化进展为HCC的可能性。随着生物医学的发展,生物信息学受到越来越多的关注,它用于检测各种疾病的特异性生物标志物,分析疾病发生和发展的分子机制。然而,目前很少有生物标志物可以预测NAFLD合并肝纤维化发生HCC的风险。因此,有必要挖掘相关生物标志物来完善这一不足。
研究方法
为了筛选出预测NAFLD进展为HCC的分子标志物,我们首先下载了GEO数据库中NAFLD合并纤维化和NAFLD相关HCC的RNA-seq数据来鉴定差异表达基因。接下来,为了探索差异表达基因的潜在功能和风险预测的关键基因,我们对两组差异表达基因的交集基因进行了GO和KEGG富集分析以及蛋白相互作用分析,还进一步地鉴定出预测NAFLD发展为HCC风险的关键基因。随后,我们对关键基因进行了Lasso Cox回归分析,以确定最适合预测NAFLD合并肝纤维化进展为HCC的基因模型。
为了评估基因模型的性能,我们利用另外两组肝脏组织测序数据进行了验证,第一组包含NAFLD合并肝纤维化和NAFLD相关HCC的测序数据,第二组包含NAFLD合并肝纤维化和NASH相关HCC的测序数据。接着,我们利用ROC曲线来展示这两个数据集对模型性能的评估结果。最后,我们利用基因模型将NAFLD患者分为HCC高危组和低危组,并对两组患者的肝脏组织测序数据进行GSEA富集分析和肿瘤免疫浸润分析。
研究结果
我们在NAFLD合并肝脏纤维化的数据集中鉴定出559个差异表达基因,在NAFLD相关 HCC的数据集中鉴定出2164个差异表达基因,交集基因共88个(图2A)。GO和KEGG富集分析显示,交集基因与活性氧应答、应激激活的MAPK级联反应、凋亡信号通路和IL-17信号通路的正调控密切相关(图2B~C)。蛋白相互作用网络将7个基因鉴定为关键基因,包括TIPM1、COL1A1、CXCL9、FOS、VWF、CD79A和VCAN,并利用7个关键基因构建基因模型(图2D)。
基因模型计算结果显示,NAFLD相关HCC数据集用于风险预测的ROC曲线下面积(AUC)为0.893,NASH相关HCC数据集用于风险预测的AUC为0.751(图2E~F)。在TCGA数据集中,用于风险预测的AUC为0.572,HCC高危组的总生存期明显短于低危组(图2G~H)。GSEA集富集分析显示PPAR信号通路、胰岛素信号通路和脂肪酸代谢在高危组显著上调,细胞内的凋亡信号通路负调控在低危组显著上调(图2I~L)。肿瘤免疫浸润分析分析显示,高危组CXCL9与巨噬细胞M1呈显著正相关,VCAN与巨噬细胞M2呈显著负相关(图2M)。
研究结论
本研究通过生物信息研究方法,鉴定出TIPM1、COL1A1、CXCL9、FOS、VWF、CD79A和VCAN为可能预测NAFLD发展为HCC风险的生物标志物。这7个基因也可能在介导NAFLD发展为HCC的潜在分子机制中发挥关键作用。
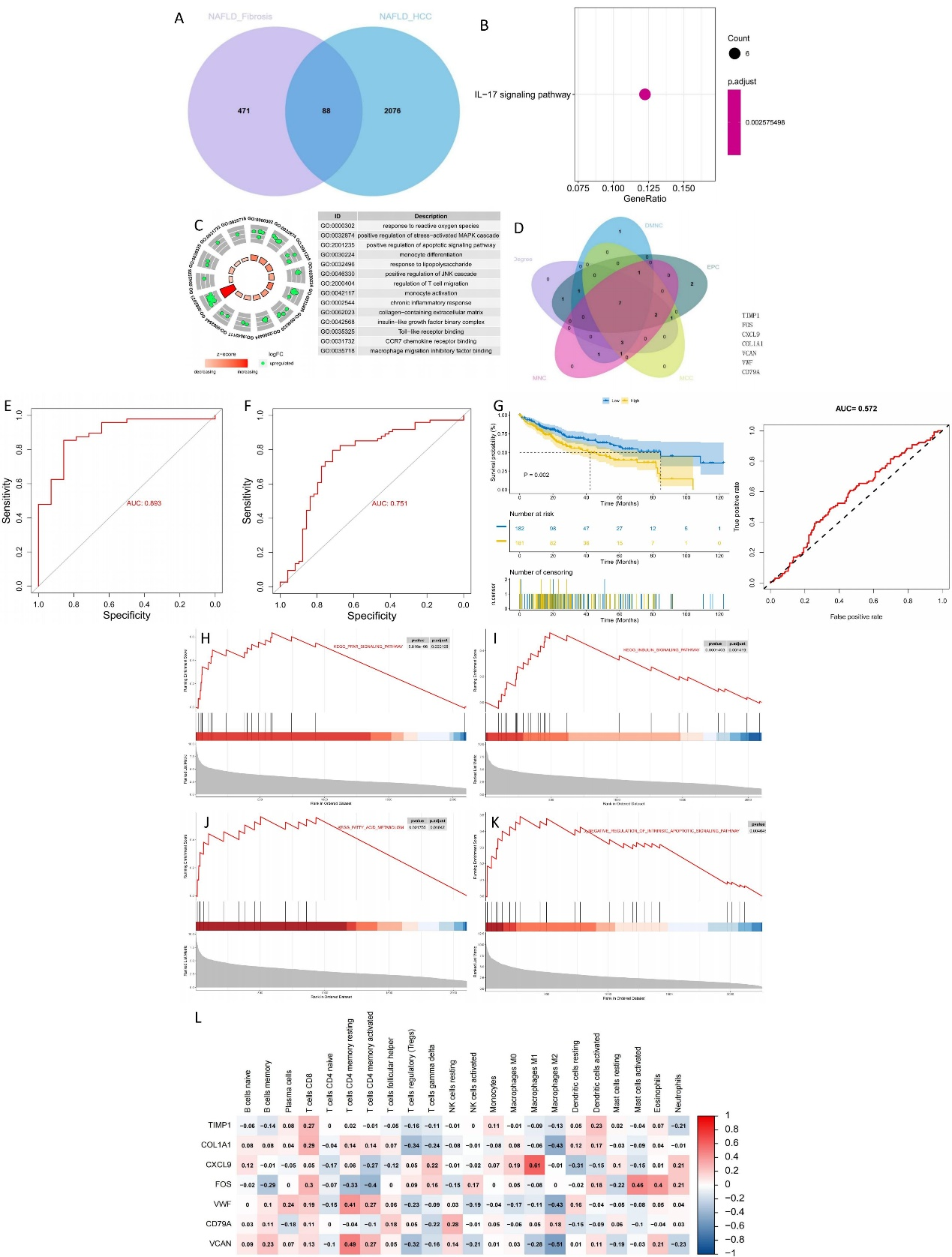
图2. 揭示可能预测NAFLD合并肝纤维化进展为HCC风险的新型关键基因
通讯作者简介

饶慧瑛
主任医师、教授,博士研究生导师。北京大学肝病研究所所长,北京大学人民医院临床试验机构副主任,丙型肝炎和肝病免疫治疗北京市重点实验室副主任。九三学社第十四届中央委员会科普工作委员会委员,首届国之名医-青年新锐,北京大学杰出青年医师。中华预防医学会促进消除病毒性肝炎工作委员会副主任委员,中华医学会肝病学分会委员、脂肪肝和酒精性肝病学组副组长,北京医学会肝病学分会副主任委员、丙型肝炎学组副组长,北京中西医结合学会肝病专业委员会副主任委员等。获得高校科技进步二等奖、北京市科技进步二等奖、中华医学科技二等奖、华夏医学科技二等奖等。擅长于难治性丙型肝炎和乙型肝炎的抗病毒治疗、脂肪肝、自身免疫性肝病、肝硬化和肝癌的诊治。
04
Drp1调控GSDMD介导线粒体功能障碍和肝细胞焦亡促进酒精性肝炎的发生
3539-C | Drp1 regulates GSDMD mediated mitochondrial dysfunction and hepatocyte pyroptosis in AH
通讯作者:谢艳迪
研究背景
近年来,全球酒精相关性疾病发病率呈上升趋势,酒精引起的肝毒性和肝损伤会导致酒精性肝病的发生。酒精性肝炎(alcoholic hepatitis,AH)是一种常见的酒精性肝病,短期死亡率较高,且目前没有有效的治疗方法。探索酒精性肝炎的发病机制对于寻找新的靶向治疗方法非常重要。在酒精性肝炎发病机制的研究中,Gasdermin D(GSDMD)激活的机制和影响尚不清楚。在目前的研究中,我们探索了动态相关蛋白1(dynamin-related protein 1,Drp1)是否调节GSDMD介导的线粒体功能障碍和肝细胞焦亡促进酒精性肝炎的发生。
研究方法
制作酒精性肝炎小鼠模型,对酒精性肝炎小鼠模型肝组织进行HE染色评估肝损伤程度,检测酒精性肝炎小鼠血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆固醇(TC)和甘油三酯(TG)水平。通过检测白介素(IL)-1β、IL-18、炎症相关蛋白和肝细胞死亡水平以评估肝细胞焦亡。通过检测线粒体DNA(mtDNA)水平、ROS生成、线粒体膜电位、ATP含量、线粒体功能相关蛋白水平和线粒体形态学变化评估线粒体功能。
研究结果
与正常小鼠相比,酒精性肝炎小鼠肝组织HE染色显示肝细胞胞质空泡和脂肪变性,中性粒细胞浸润的灶状坏死和肝窦充血,提示酒精性肝炎小鼠更严重的肝损伤。酒精性肝炎小鼠血清中AST、ALT、TC和TG水平显著增加。酒精性肝炎小鼠血清中IL-1β、IL-18水平显著增加。酒精性肝炎小鼠肝组织中GSDMD-N、NLRP3和Caspase-11蛋白表达的增加提示GSDMD激活。下调GSDMD能够减轻酒精导致的肝细胞焦亡。酒精性肝炎小鼠肝组织中可以看到酒精导致肝细胞的线粒体功能障碍,当下调GSDMD后这一现象得到改善。改善线粒体功能后也能抑制酒精导致的肝细胞焦亡。GSDMD或Drp1敲除改善了酒精性肝炎的肝损伤,同时伴随着肝细胞焦亡的减轻。
研究结论
在酒精导致的肝脏炎症和肝脏损伤的过程中,Drp1调节GSDMD介导的线粒体功能障碍和肝细胞焦亡。这些发现可能为研发新的酒精性肝炎治疗方法奠定基础。
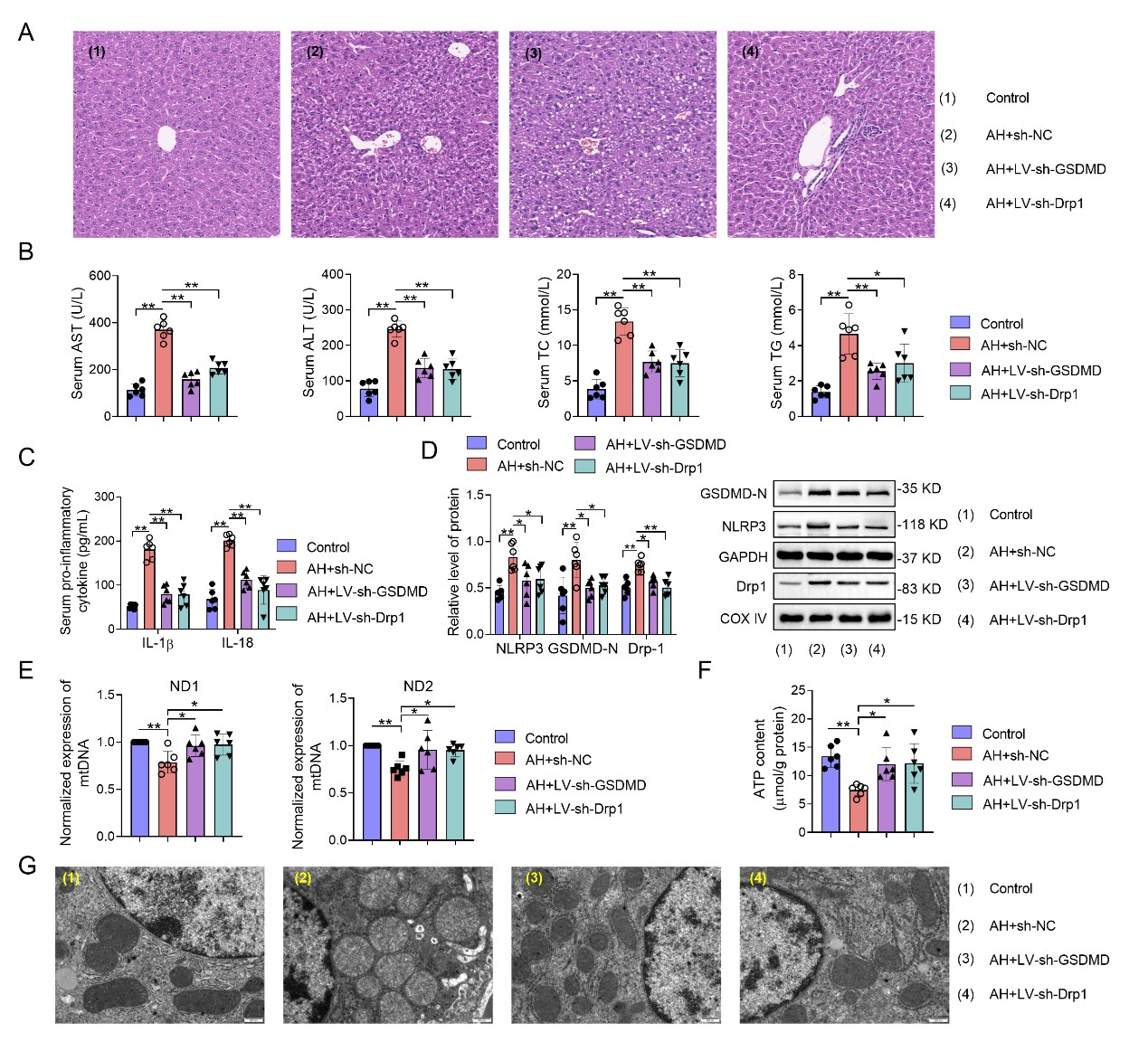
图3. Drp1调控GSDMD介导线粒体功能障碍和肝细胞焦亡促进酒精性肝炎的发生
通讯作者简介

谢艳迪
医学博士,副主任医师。毕业于北京大学医学部,现就职于北京大学人民医院肝病科、北京大学肝病研究所。中华医学会肝病学分会肝病相关消化病协作组成员。中华医学会肝病学分会肝病基础医学与实验诊断协作组成员。主持国自然青年基金1项、北京大学人民医院院内基金3项,发表SCI文章9篇。先后获得北京大学优秀毕业生、北京市优秀毕业生、北京大学人民医院青年教师教学比赛二等奖、北京大学医学部传染病学系青年教师教课比赛一等奖、肝病临床思维训练营全国总决赛优胜奖、多次获得学术会议优秀论文一等奖及青年研究者奖。专业特长为各种肝脏疾病的诊断和综合治疗,研究方向为酒精性肝炎的发病机制、慢乙肝的临床治愈。
会场花絮




声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
标签:
研究
热点聚焦
其他肝病
发表评论
全部评论