当前位置:AASLD-美国肝病研究学会年会 » 正文
肝愈之道——聚焦AASLD热点学术进展,看慢乙肝治疗的“中国力量”
—— 作者: 时间:2021-11-26 11:53:04 阅读数:
42
编者按:第72届美国肝病研究学会(AASLD)年会于2021年11月12日至15日以虚拟数字会议的形式召开,这也是2021年肝病学领域的年度压轴盛会。作为患者群体最多、对人类健康威胁最大的肝脏疾病之一,慢性乙型肝炎(CHB)等病毒性肝炎仍是会议关注焦点,而特别值得一提的是,本次AASLD年会的CHB相关学术分享有许多来自中国中青年学者,让我们看到了CHB治疗的“中国力量”正在不断加速崛起。
为了近距离感受“新势力”的学术风采,《国际肝病》在AASLD年会期间策划并组织了以“AASLD超速圆桌会·见证中国年轻力量的崛起”为主题的学术直播活动,本次直播邀请到重庆医科大学附属第二医院胡鹏教授主持会议,同时邀请到南京大学医学院附属鼓楼医院黄睿教授、天津市第二人民医院陈鹏教授、首都医科大学附属北京佑安医院李磊教授、青岛大学附属医院饶伟教授,以及郑州大学第一附属医院曾庆磊教授,分别带来精彩的报告分享。现将本次圆桌会的学术报告精华内容整理如下,供各位读者学习参考。
重视ALT正常、HBV DNA阳性CHB患者的肝组织炎症
南京大学医学院附属鼓楼医院黄睿教授介绍了其团队在本次AASLD发表的一项对ALT正常、HBV DNA阳性CHB患者的肝组织炎症分布回顾性分析[1],共纳入2个中心581例CHB患者活检样本,评价显著肝组织炎症比例以及患者HBV DNA水平等因素的影响,研究设计具体如图1所示。

图1.对ALT正常、HBV DNA阳性亚洲CHB患者的肝组织炎症回顾性分析的设计
研究显示,肝脏纤维化越严重、ALT水平越高,患者肝组织炎症越严重,其中肝硬化患者大部分存在严重肝组织炎症,即使ALT<正常参考值上限(ULN)的患者,存在中-重度肝组织炎症的比例也超过80%;但ALT正常、无显著肝纤维化的HBV DNA阳性患者中,同样有28.7%存在显著肝组织炎症(Scheuer评分G≥2,见图2),可能需积极抗病毒治疗。
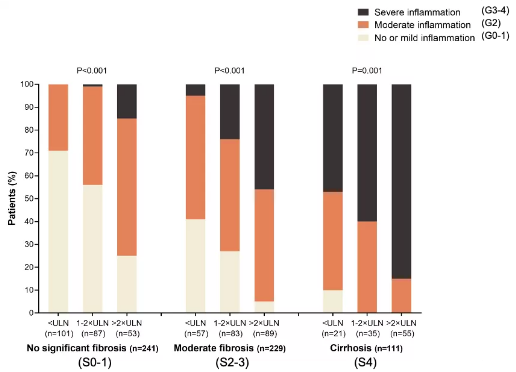
图2.ALT水平、肝纤维化水平与HBV DNA阳性CHB患者肝组织炎症的关系
不同HBeAg状态的患者,肝组织炎症均随纤维化程度加重而加重;而在相同纤维化程度的CHB患者中,肝组织炎症程度随ALT水平升高而加重(见图3),但不论患者HBeAg状态如何,年龄≥40岁或<40岁,均有约30%无显著纤维化、ALT水平正常的患者存在显著肝组织炎症,是临床应高度关注的人群。
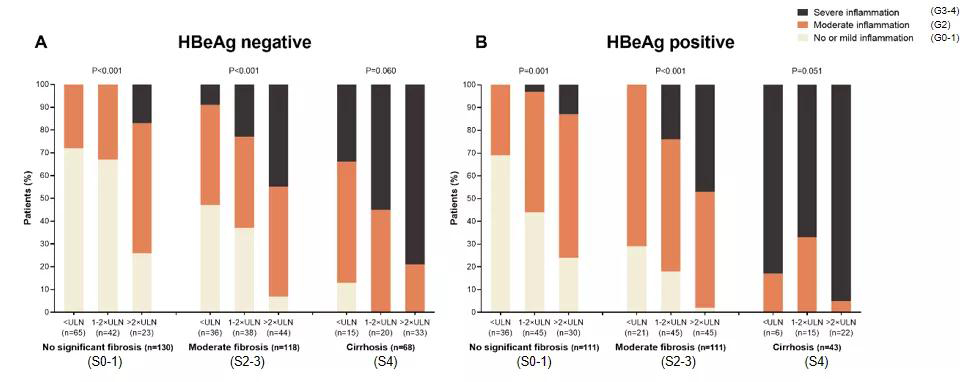
图3.不同HBeAg状态与HBV DNA阳性CHB患者肝组织炎症的关系
不同HBV DNA载量的CHB患者,肝组织炎症程度的分布也有不同,中等水平HBV DNA(5-7 log10 IU/mL)患者显著肝组织炎症程度最高;而在同等HBV DNA水平下,ALT水平越高,患者肝组织炎症越重(见图4)。
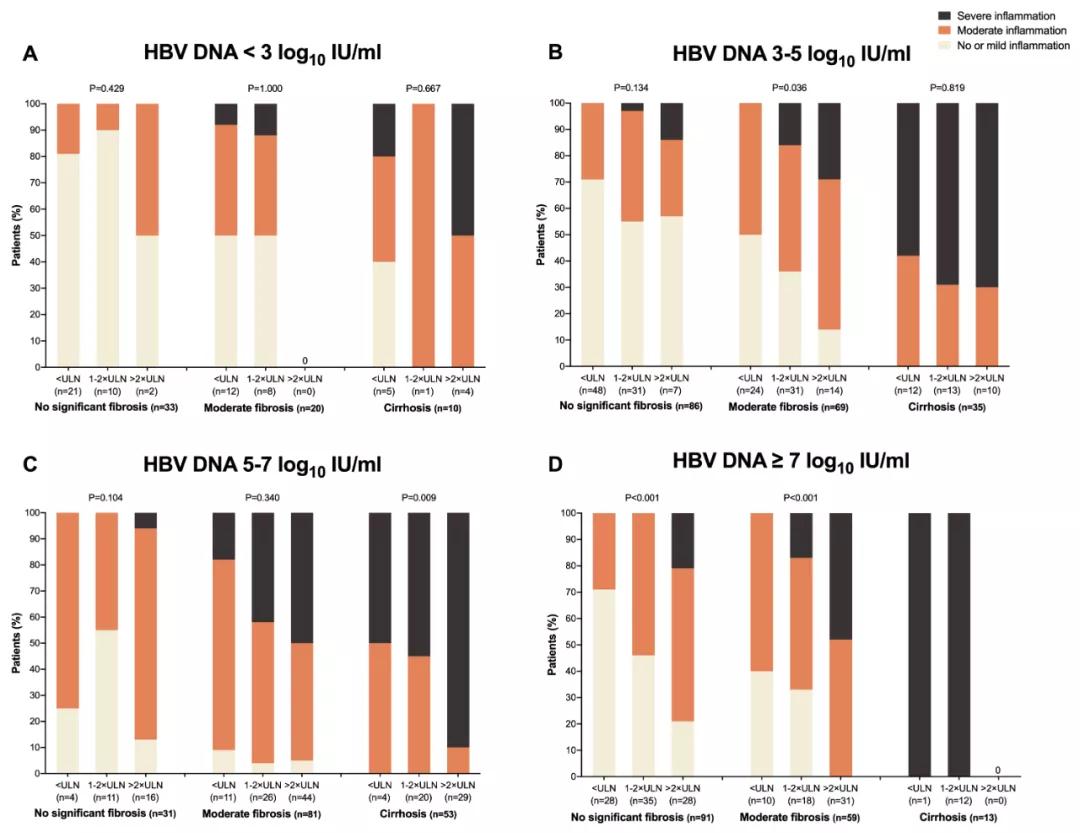
图4.不同HBV DNA载量的CHB患者肝组织炎症程度分布
多因素分析显示,中等水平HBV DNA是ALT正常、无显著肝纤维化下,HBV DNA阳性CHB患者显著肝组织炎症的主要风险因素(调整后OR: 13.161,95% CI:1.026-168.889,P=0.048),对此类患者必要时应行穿刺评估炎症,积极进行抗病毒治疗。
TAF在初治及合并NAFLD的CHB人群中应用状况
天津市第二人民医院陈鹏教授也分享了所在团队在本届AASLD年会上发表的两项真实世界研究,分别是应用2019年我国《慢性乙型肝炎防治指南》推荐的CHB治疗一线用药丙酚替诺福韦(TAF)[2],治疗核苷(酸)类似物(NAs)初治及合并NAFLD的初治CHB患者。
第一项研究共纳入118例初治CHB患者[3],除评估TAF在治疗24、48和96周的病毒学/生化学应答率等疗效指标外,还对病毒学应答相关预测因子进行分析。病毒学应答方面,24周时患者平均HBV DNA显著低于基线[(1.62±1.03)lg IU/mL vs. (5.42±1.98)lgIU/mL],完全病毒学应答(CVR,HBV DNA<20 IU/mL)率为49.0%;48周时患者平均HBV DNA降至1.21±0.67 lgIU/mL,显著低于24周时水平(见图5),CVR率为71.19%。
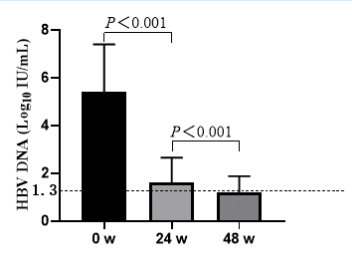
图5.TAF治疗初治CHB患者24、48周时的平均HBV DNA水平
20例随访至96周的患者中,85.0%(17/20)HBV DNA已检测不到,同时在治疗24周和48周时,患者HBsAg水平都较基线显著下降(P<0.05)。多因素logistic回归分析显示,患者基线时的HBsAg水平是影响TAF治疗48周病毒学应答的独立危险因素(OR=2.458,95% CI:1.008-5.995, P=0.048)。
生化学应答方面,患者基线的ALT、AST异常率分别为55.08%和49.15%,TAF治疗24周后,异常率分别下降至10.64%和7.45%,48周后进一步显著下降至8.33%和2.38%(见图6,研究采用的ALT正常值上限为40 U/L,AST正常值上限为35 U/L)。
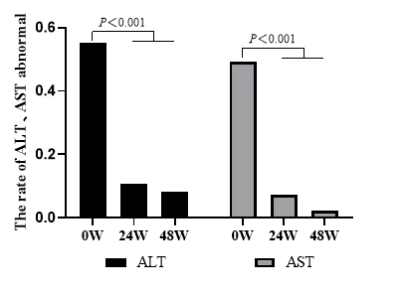
图6.初治CHB患者ALT、AST水平在24、48周时较基线的变化情况
患者肝脏硬度值(LSM)从基线的12.35±9.83kPa,显著下降至48周的8.04±4.01kPa(P=0.001),受控衰减参数(CAP)和估算肾小球滤过率(eGFR)在24周和48周时较基线无显著改变(P>0.05),提示TAF治疗可一定程度上改善肝纤维化,且肾脏安全性较好。
第二项研究共分析86例核苷(酸)类似物初治CHB患者,其中38例(44%)为合并NAFLD的患者(A组),评估TAF治疗的效果和NAFLD对疗效的影响[4]。
生化学应答方面,A组患者基线的ALT异常率(研究采用ALT正常值上限为40 U/L)为71.05%,B组(仅有CHB而无NAFLD,n=48)的ALT异常率为58.33%;TAF治疗24周和48周后,A组的ALT复常率分别为74.07%和84.62%,B组分别为92.86%和86.96%,两组在同一时间点ALT复常率差异无统计学意义(P>0.05),提示无论患者是否合并NAFLD,TAF治疗均可有效提升ALT复常率,稳定肝功能。
TAF治疗后24周,B组的CVR(HBV DNA<20 IU/mL)率显著高于A组 (58.2% vs. 34.2%),但在48周时两组间CVR率差异无统计学意义(75.5% vs. 72.2%,见图7),提示无论初治CHB患者是否合并NAFLD,TAF治疗均可有效抑制HBV DNA复制,且单因素logistic回归分析显示,NAFLD不是48周时TAF抗病毒治疗失败的危险因素(OR=2.196,95% CI:0.817-5.900,P>0.05)。

图7.患者治疗24、48周时的HBV DNA水平
TAF治疗后48周,两组患者平均HBsAg水平低于基线[(3.23±0.65)lgIU/mL vs. (3.70±0.76) lgIU/mL,P<0.05],LSM显著降低[8.8 (6.4,14.8)kPa vs. 6.75(5.25,8.73)kPa,P<0.05],且组间差异无统计学意义(P>0.05),提示无论初治CHB患者是否合并NAFLD,TAF治疗均可降低患者HBsAg水平,改善肝纤维化。
TAF在失代偿期乙肝肝硬化,且其他NAs应答不佳或存在低病毒血症患者中的应用
首都医科大学附属北京佑安医院李磊教授介绍了所在团队于本届AASLD发表的一项前瞻性研究[5],研究以TAF 25 mg QD单药治疗,用于56例既往使用其他NAs治疗至少6个月,但应答不佳(定义为从其他NAs治疗换用TAF时,HBV DNA≥2000 IU/mL,共30例)或有低病毒血症(LLV,定义为换用TAF时,HBV DNA超敏检测阳性但<2000 IU/mL,共26例)的失代偿期肝硬化CHB患者,患者部分基线特征及既往治疗情况见图8。
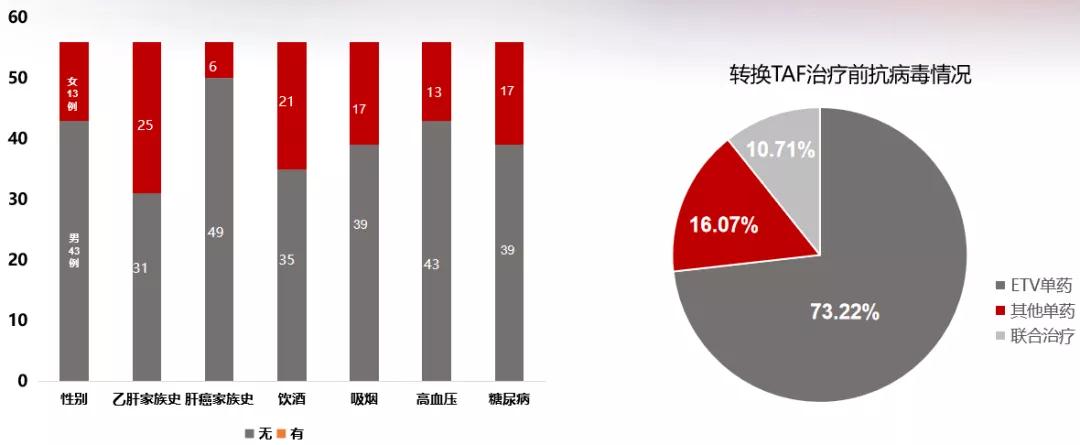
图8.研究中患者的部分基线特征
研究对患者每12周进行一次评估,换用TAF治疗后12、24、36、48周,ALT复常率均在90%以上,较基线的66%均显著增高(P<0.05),且各个评估节点的复常率之间差异无统计学意义;患者治疗48周时的平均Child-Pugh评分为5.45±0.76,Child A级患者占85%,显著优于基线时的8.66±2.30和21.43%(P<0.05)。患者CVR率随着治疗时间延长而上升,至治疗48周时达到80%,显著高于12周时的32.14%(P<0.05,见图9)。
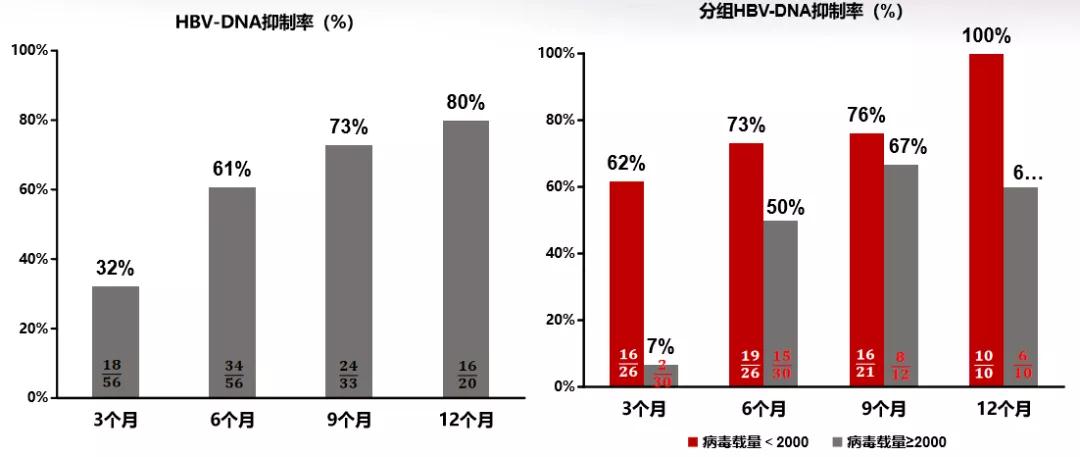
图9.患者整体及LLV组/应答不佳组的HBV DNA抑制情况
基线为LLV的患者,治疗12周时的CVR比例较应答不佳患者更高(61.54% vs. 6.67%),但24/36/48周时两组CVR比例无显著差异(见图10)。治疗期间患者血清HBsAg定量及HBV DNA水平均进行性下降,至治疗48周时平均HBsAg定量较基线显著下降0.44 log IU/mL,平均HBV DNA水平较基线显著下降3.88 log IU/mL(P<0.05)。
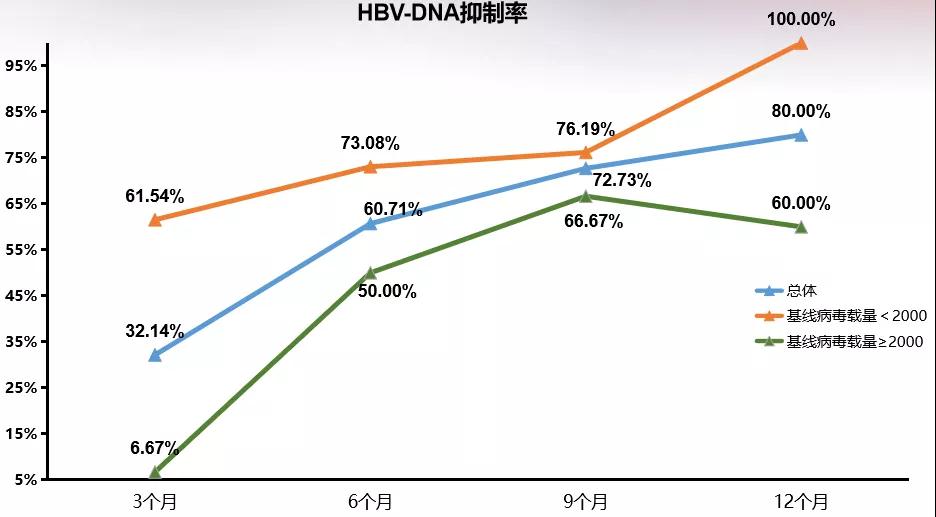
图10.不同时间节点两组患者的HBV DNA抑制率
48周治疗期间,患者肌酐、血清磷酸酶、eGFR等肾脏安全性指标较基线均无显著改变(P>0.05),尿β2微球蛋白(β2-MG)较基线呈下降趋势(24周时均值为0.98,较基线时的1.14有所下降,但未达统计学显著性)。上述数据显示,TAF单药治疗其他NAs应答不佳或低病毒血症的失代偿期肝硬化CHB患者可改善病毒抑制情况,且肾脏安全性良好。
重视对肝移植患者HBV感染的管理
青岛大学附属医院饶伟教授介绍了两项与肝移植患者HBV感染有关的研究。第一项为来自新西兰的开放标签、临床II期研究[6],评估伴慢性肾病患者肝移植后,使用TAF预防HBV感染4年的疗效与安全性,研究整体设计如图11所示,患者先按1:1比例分别在48周内继续使用富马酸替诺福韦酯(TDF)或换用TAF预防,此后开放标签阶段均使用TAF预防。

图11.新西兰临床II期研究设计(HBV DNA最低检测标准为<20 IU/mL)
数据显示,不论患者在48周内使用TDF还是TAF预防,后续至治疗192周时HBV DNA的持续病毒学控制率均为100%;随机对照期间TAF组的任意级别不良事件发生率为92%,略低于TDF组的96%,3-4级不良事件发生率为8%对24%,严重不良事件发生率为12%对28%,两组均无3-4级药物相关不良事件,开放标签阶段随访结果提示相似的安全性。
骨肾安全性指标显示,TAF组患者治疗192周时,eGFR较基线上升3.5 mL/min/1.73m2,(Q1,Q3: -1.2,7.7),数值上略高于TDF组的1.1 mL/min/1.73m2(Q1,Q3: -6.3,9.0),且TDF组患者换用TAF后,eGFR可升高并保持稳定;TAF治疗还可维持患者脊柱/髋骨密度,治疗192周时患者两处骨密度均较基线有所上升;TDF组患者在48周随机对照研究期间脊柱/髋骨密度降低,而换用TAF后患者骨密度回升。
第二项则是饶伟教授所在中心的单中心分析[7],发现患CHB肝移植受者的LLV与HCC复发相关,该研究共纳入49例存在CHB相关并发症的肝移植受者,以高敏HBV DNA检测结果分为CVR组(HBV DNA≤10 IU/mL,n=43)或LLV组(HBV DNA≥10 IU/mL,n=6),评估肝移植后患者的LLV发生率及相关影响因素,研究完整设计及入排标准如图12所示。

图12.研究设计及入排标准
从患者基线特征来看,分析时患者中位移植后时间为36个月,CHB相关并发症为肝细胞癌(HCC)的患者占57%(28/49),31例患者移植前接受抗病毒治疗,其中23例使用恩替卡韦(ETV);患者术后末次随访时的抗病毒方案为NAs单药或NAs+乙肝免疫球蛋白(HBIG,两种方案各占约50%),其中NAs用药以ETV(30例)、TAF(15)例为主。
6例LLV患者中5例移植前原发病为HCC,目前3例尚无肿瘤复发或转移;5例患者移植术前HBV DNA阳性。分析显示,BMI及总胆红素偏低、肝移植前HCC分期超UCSF标准及HCC复发或转移,为肝移植后LLV发生的相关因素(见表1),其中原发病为HCC的患者,CVR组23例中仅1例有HCC复发,而LLV组5例中有2例复发,提示应对复发风险较高的HCC患者行动态高敏监测,使用TAF等药物及时干预LLV以改善患者长期预后。
表1.肝移植后LLV发生的相关因素

TAF在活动期CHB孕妇治疗和HBV母婴阻断中的应用
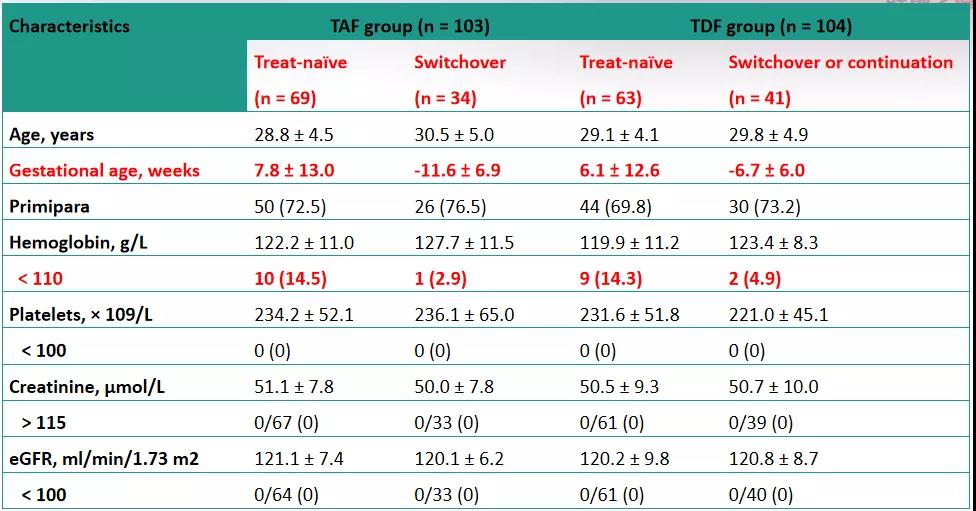
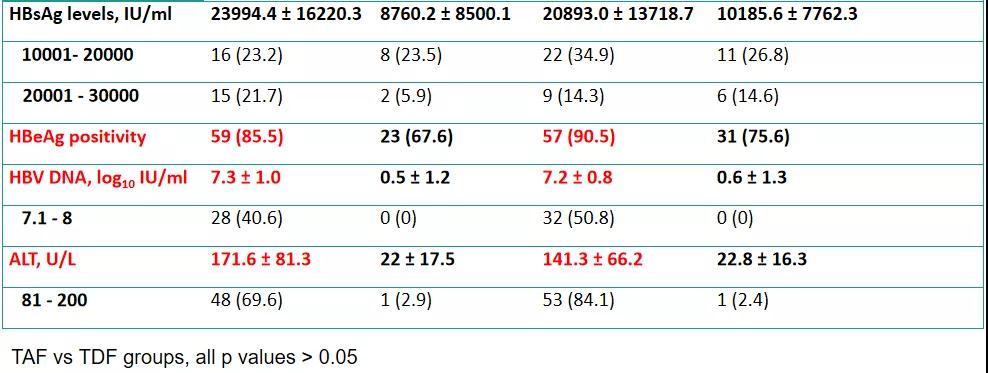
郑州大学第一附属医院曾庆磊教授汇报了一项以TAF治疗活动性CHB孕妇、阻断HBV母婴传播的多中心、前瞻性、真实世界对照研究。该研究入选本届AASLD年会的口头报告[8],共纳入207例新诊断或既往有活动性CHB诊断的孕妇,根据患者意愿按1:1分组予TAF或TDF治疗,并按标准处理方式以HBIG+HBV疫苗行母婴阻断,评估TAF治疗的安全性,如围术期不良事件发生率、并发症、肝肾功能和疗效,起始治疗时孕妇的基线特征见表2。
表2.TAF/TDF治疗孕妇患者的基线特征
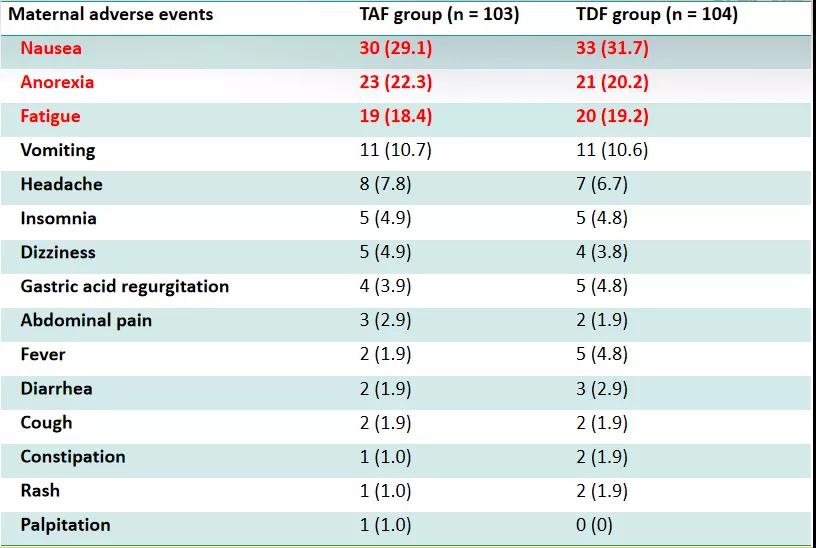
TAF或TDF用于孕妇活动性CHB治疗的安全性好,恶心、乏力、厌食等不良事件的发生率相当(见表3),胎膜早破、早产等围产期并发症发生率也相当。两组婴儿出生时均无先天缺陷或畸形,也无明显的异常症状;TAF组有一例孕妇治疗4周内HBV DNA定量就较基线时下降4 log10 IU/mL,但因孕22周时首次超声检查发现唇腭裂而决定终止妊娠,经咨询专科医生及查阅文献,初步判定唇腭裂与TAF治疗无关。
表3.治疗期间CHB孕妇的不良事件
出生婴儿随访7个月、12个月、18个月时,生长发育指标均正常,HBsAg检测均为阴性,母婴传播率为0;而CHB孕妇接受TAF治疗后,不论是初治还是从其他NAs换用TAF,随访12个月、18个月时的HBV DNA无法测得比例均达到100%(见图13),ALT复常率也在治疗18个月时达到94.7-100%,但也有2例TAF组经治孕妇发生病毒学突破,其中一例加用拉米夫定后控制良好;初治组/经治组孕妇HBeAg转换率均相似。
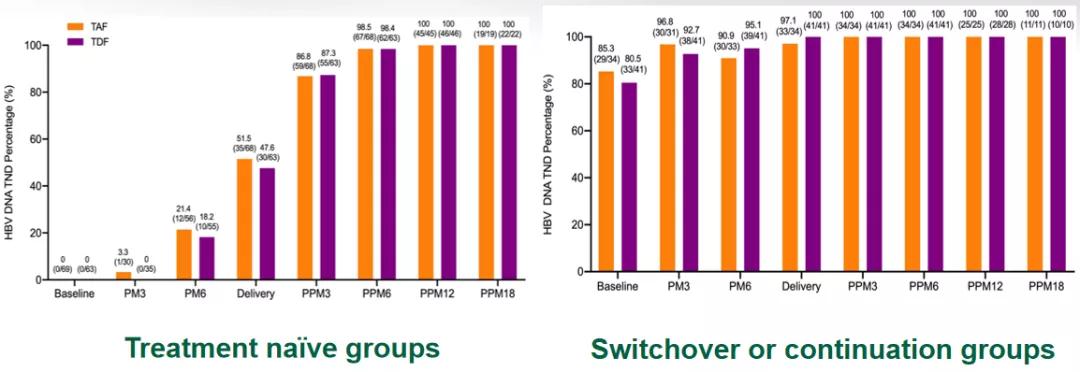
图13.初治和经治孕妇使用TAF/TDF治疗后的病毒学抑制情况
总体来看,TAF和TDF治疗活动性CHB孕妇2年的表现整体相当,均为安全性、有效性良好的治疗手段,现有标准母婴阻断方式上加用TAF,能将HBV母婴传播率降为0。
总 结
本届AASLD年会上来自中国学者的CHB相关研究可谓精彩纷呈。圆桌会上分享的各项研究全面评估了TAF在初治、合并NAFLD、肝移植受者、失代偿期肝硬化等CHB人群中的应用情况,TAF治疗整体表现出良好的安全性和有效性,对复杂多样的临床患者情况适应较好,将继续成为临床工作者的CHB抗病毒治疗利器。
参考文献:
1. Liu J, et al. AASLD 2021, Poster 718.
2. 中华医学会感染病学分会,等. 中华传染病杂志. 2019;37(12):711-736.
3. Chen P, et al. AASLD 2021, Poster 782.
4. Chen P, et al. AASLD 2021, Poster 791.
5. Juan A, et al. AASLD 2021, Poster 824.
6. Edward J et al. AASLD 2021, Poster 803.
7. Rao W, et al. AASLD 2021, Poster 1541.
8. Zeng Q, et al. AASLD 2021, Oral 19.
标签:
研究
热点聚焦
乙肝
发表评论
全部评论
