当前位置:EASL-欧洲肝脏研究协会年会 » 正文
EASL2019丨如何克服肝癌治疗中的索拉非尼耐药问题——浙江邵逸夫医院蔡秀军教授团队发现两个潜在靶点
—— 作者: 时间:2019-04-24 05:17:31 阅读数:
448

中国是乙型肝炎大国,约有8000万患者,即全球1/3的乙型肝炎人群在中国。得益于上世纪90年代起实施的HBV疫苗计划,目前中国5岁以下儿童的HBV感染率仅有1%,但是从HBV感染率降低到肝癌发病率降低还需要一定时间。目前,肝细胞肝癌(hepatocelluar carcinoma,HCC)还是中国第四常见的恶性肿瘤和第三大肿瘤致死因素。
浙江大学医学院附属邵逸夫医院蔡秀军教授团队对HCC治疗中所面临的索拉非尼耐药问题进行了探索,发现了两个潜在治疗靶点(蛋白UBQLN1和circRNA-RUSH)。季琳博士代表团队于第54届欧洲肝脏研究学会年会(EASL2019)的平行会议上对这一发现进行了介绍(摘要编号:PS-114),并应《国际肝病》邀请将研究思路及重要发现分享如下。
季琳博士在EASL/ILC2019现场
研究背景:
在过去十年中,索拉非尼是唯一一个被批准用于治疗晚期肝癌的分子靶向药物。在两项大型临床试验SHARP和第三阶段的索拉非尼亚太(AP)试验中,索拉非尼能有效改善患者的预后。然而,索拉非尼带来的这种益处是很有限的。由于治疗过程中常发生耐药,患者的中位存活时间仅能延长大约3~5个月。
既往研究发现耐药机制主要包括ERK和PI3K等与细胞存活相关通路上蛋白表达的异常。同时,自噬、上皮间质转化(epithelial-mesenchymal transition,EMT)、缺氧相关蛋白也与索拉非尼耐药有关。最近的一些研究发现线粒体可能也是索拉非尼的作用靶点之一。
考虑到活性氧(reactive oxygen species,ROS)在药物疗效反应中常发挥关键作用,而线粒体不仅与细胞凋亡密切相关,也是细胞内ROS的主要来源。所以我们就想探究看线粒体在索拉非尼耐药的发生发展中承担了一个什么样的角色。肝癌细胞是如何对抗线粒体损伤和ROS增加而产生耐药的呢?
主要过程和发现:

图1 UBQLN1和circRNA-RUSH参与的索拉非尼耐药机制
首先通过长期暴露缓慢增加的索拉非尼,我们构建了3对索拉非尼耐药的细胞系。然后我们检测了这些细胞在索拉非尼处理和不处理条件下的ROS水平。我们发现在野生型HCC细胞系中,索拉非尼治疗可以增加细胞内ROS水平。然而,在耐药性细胞系中,索拉非尼治疗后细胞内ROS水平却降低了。
通过流式细胞术测试,药物处理后耐药细胞中线粒体跨膜电位的降低较野生型细胞少。 透射电镜(Transmission electron microscope,TEM)结果也显示野生型细胞系中,线粒体的变形程度更大,而耐药性细胞中的线粒体似乎能保持更完整的形态。考虑到细胞可能通过自噬,降解受损的线粒体,所以细胞发生的自噬水平也能侧面反映细胞内受损的线粒体情况。我们在药物处理下检测了耐药和野生型细胞中的自噬水平,发现耐药性细胞中的自噬水平较低,这与耐药性细胞中线粒体损伤程度低是相符合的。
为了进一步研究其背后的机制,我们采用了环状RNA芯片检测(Arraystar Human CircRNA Array),发现并命名circRNA-RUSH(Resistance Upregulated in Sorafenib treated HCC patients)在HepG2 耐药细胞中明显增加。通过siRNA转染技术减少该circRNA可以增加细胞内ROS水平,降低线粒体跨膜电位,并诱导自噬。而ROS抑制剂,N-乙酰半胱氨酸(N-Acetylcysteine,NAC)能部分地挽救由circRNA减少诱导的细胞凋亡。因此,我们认为索拉非尼耐药细胞中这种circRNA的增加可以增强细胞对线粒体损伤和ROS的耐受。
为了更好地证明我们的理论,我们进行了质谱检测以筛选可能的作用分子。有趣的是,质谱结果的Gene Ontology(GO)分析显示该circRNA降低后,线粒体相关蛋白发生了富集。由于过去有研究表明,线粒体受损可能会导致某些错位的线粒体蛋白的增加,而错位的线粒体蛋白又与细胞内ROS水平之间存在可能的联系。所以这个GO分析的结果也是对我们的理论的一个很好的证明。同时KEGG分析也显示代谢相关通路在该circRNA降低后发生了富集。
然后通过RNA pulldown的技术,我们获得了与该circRNA结合的蛋白,并对该circRNA结合的蛋白进行了另一个质谱检测。通过比较这两次的质谱结果,我们发现UBQLN1蛋白出现在pulldown组中,这表明它可能与该circRNA有结合。既往文献报道UBQLIN1蛋白能帮助错位的线粒体蛋白的降解。也有文献支持UBQLN1能减少ROS对细胞的损伤。同时在上一个质谱结果中也提示该蛋白在circRNA减少后发生了降低。所以我们假设circRNA-RUSH能稳定该蛋白,而行使功能。
为了验证这个假设,我们进行了RNA免疫共沉淀,RNA pulldown后的western blot检测和共定位荧光显微镜检测(图2)。实验结果与我们的假设相符。这些结果证明该蛋白与circRNA相互结合。
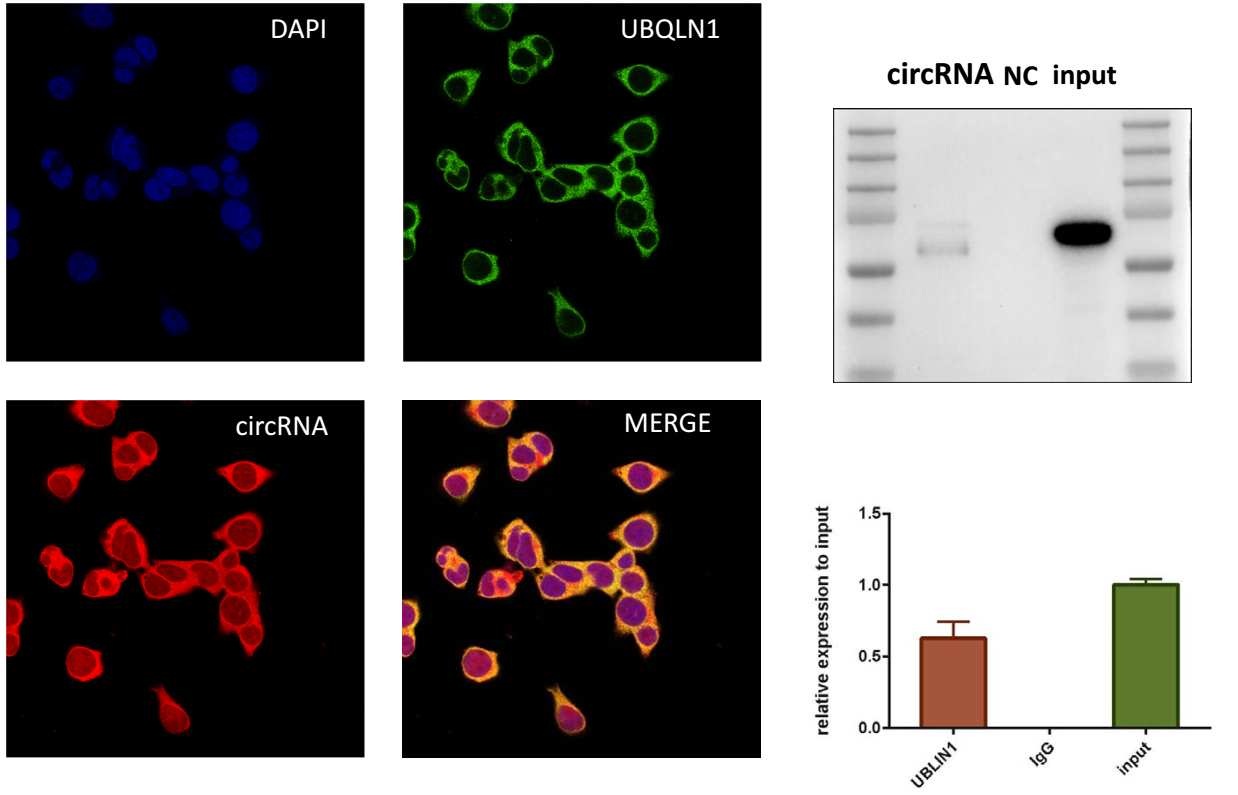
图2 UBQLN1与circRNA相互结合
而后,我们又通过western blot实验比较UBQLN1蛋白在耐药细胞和野生型细胞中表达的差异,发现耐药细胞中该蛋白表达较野生型细胞高。而减少circRNA-RUSH可加速该蛋白的降解(图3)。

图3 耐药细胞中circRNA-RUSH的减少加速UBQLN1蛋白降解
通过siRNA转染使UBQLN1沉默后,细胞内ROS水平升高,线粒体跨膜电位降低。另外,实验也发现过表达UBQLN1蛋白能部分地挽救由circRNA消耗诱导的一些细胞凋亡(图4)。

图4 过表达UBQLN1蛋白能部分地挽救由circRNA消耗诱导的细胞凋亡
小结与展望:
这项研究还有许多工作要做。首先,过表达蛋白质UBQLN1无法挽救所有由circRNA降低引起的死亡。因此,我们认为可能这种circRNA对索拉非尼耐药性的贡献可能还存在其他机制。第二,单个circRNA可能不能完全解释我们构建的这些细胞系中产生的索拉非尼耐药性的机制。所以还需要进一步研究。但是,我们认为目前的实验结果可以很好地证明蛋白UBQLN1和circRNA-RUSH确实参与了这一过程。因此,它们可能是克服索拉非尼耐药的潜在靶点。
标签:
传真
热点聚焦
肝癌
发表评论
全部评论